Grignardove činidlá, objavené francúzskym chemikom Françoisom Augustom Victom Grignardom na prelome 20. storočia, predstavujú jeden z najvýznamnejších nástrojov v arzenáli organickej syntézy. Nobelova cena udelená v roku 1912 za objav týchto organohorečnatých zlúčenín svedčí o ich revolučnom vplyve na modernú chémiu. Grignardova reakcia, ako sa proces prípravy a následného využitia týchto činidiel nazýva, nesmierne zjednodušila a sprístupnila tvorbu nových väzieb uhlík-uhlík, ako aj väzieb uhlíka s heteroatómami ako fosfor či kremík. Mimoriadne dôležité je ich využitie pri syntéze sekundárnych a predovšetkým terciárnych alkoholov, čo je oblasť, ktorá bude v tomto článku podrobnejšie preskúmaná.
Štruktúra a príprava Grignardových činidiel
Grignardovo činidlo je všeobecný názov pre chemické zlúčeniny, ktorých všeobecný vzorec je R-Mg-X, kde X predstavuje halogén (typicky chlór, bróm alebo jód) a R je organická skupina, či už alkylová alebo arylová. Medzi typické príklady patria metylmagnéziumchlorid (CH3MgCl) a fenylmagnéziumbromid (PhMgBr). Hoci sa často zapisujú v lineárnej forme R-Mg-X, v skutočnosti, keď je činidlo rozpustené v Lewisovej báze, horčík nadobúda tetrahedrálnu geometriu. Tieto zlúčeniny patria do širšej kategórie organohorečnatých zlúčenín.
Príprava Grignardovho činidla obvykle zahŕňa reakciu kovového horčíka s organickým halogenidom, najčastejšie organobromidom, v bezvodom éterovom rozpúšťadle, ako je dietyléter alebo tetrahydrofurán (THF). Éter je nevyhnutný na stabilizáciu organohorečnatých zlúčenín. Proces prípravy nie je okamžitý a vyžaduje si tzv. indukčnú periódu. Počas tejto počiatočnej fázy sa odstraňuje vrstva oxidu, ktorá prirodzene pasivuje povrch kovového horčíka. Po prekonaní tejto pasivácie sa reakcia stáva vysoko exotermickou.
Horčík sa prirodzene pokrýva vrstvou oxidu horečnatého (MgO), čo je proces známy ako pasivácia. Táto vrstva bráni ďalšej reakcii s organickými halogenidmi. Na oslabenie alebo odstránenie tejto vrstvy existuje viacero metód. Mechanické metódy zahŕňajú drvenie horčíka na menšie kúsky, intenzívne miešanie alebo použitie ultrazvuku (sonikácia). Chemická aktivácia sa dosahuje pridaním malého množstva aktivačných látok, ako je jód, metyljodid alebo 1,2-dibrómetán. Tieto látky reagujú s povrchom horčíka a odstraňujú pasivačnú vrstvu. Množstvo spotrebovaných aktivačných látok je zvyčajne zanedbateľné. Alternatívou je použitie malého množstva chloridu ortutnatého, ktorý vytvorí na povrchu horčíka amalgám a zvýši jeho reaktivitu. Špeciálne pripravené formy horčíka, napríklad Riekeho horčík, obchádzajú problém pasivácie úplne.
Mechanizmus reakcie Grignardovho činidla
Okrem priamej reakcie horčíka s organickým halogenidom existujú aj alternatívne metódy prípravy. Jednou z nich je prenos atómu horčíka z už pripraveného Grignardovho činidla na iný organický halogenid. Táto metóda má výhodu v tom, že toleruje prítomnosť mnohých funkčných skupín. Ďalším spôsobom je reakcia horčíka s organozinočnatými zlúčeninami. Touto cestou sa podarilo pripraviť aj Grignardove činidlá na báze adamantánu, ktorých syntéza bežnými metódami je komplikovaná kvôli možným vedľajším reakciám.
Keďže Grignardove činidlá sú extrémne citlivé na vlhkosť a kyslík, ich skladovanie a manipulácia vyžadujú špeciálne podmienky. Normálne sa uchovávajú vo forme roztokov v éterických rozpúšťadlách, kde sú stabilné, pokiaľ nedôjde ku kontaminácii vodou. Existuje niekoľko metód na overenie ich kvality a koncentrácie, vrátane titrácie s bezvodými protickými činidlami, ako je mentol, v prítomnosti indikátora.
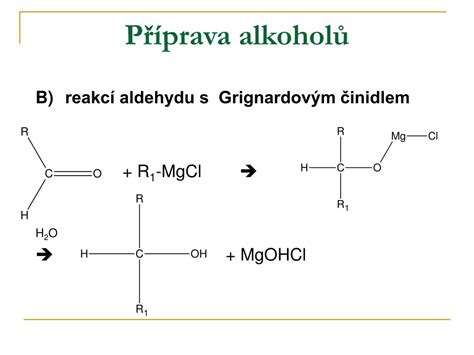
Grignardova reakcia s karbonylovými zlúčeninami: Cesta k alkoholom
Grignardove činidlá sú nukleofily, čo znamená, že majú tendenciu atómový útok na elektrónovo deficitné centrá. V organickej syntéze je ich najvýznamnejšou aplikáciou reakcia s karbonylovými zlúčeninami - aldehydmi a ketónmi. Táto reakcia je kľúčová pre syntézu alkoholov, vrátane terciárnych.
Proces prebieha nasledovne: do roztoku Grignardovho činidla (R-Mg-X) sa pridá karbonylová zlúčenina (aldehyd R'CHO alebo ketón R'COR''). Uhlík v karbonylovej skupine (C=O) je čiastočne kladne nabitý (δ+) v dôsledku elektronegativity kyslíka, čo ho robí náchylným na nukleofilný atak. Nukleofilný uhlíkový atóm Grignardovho činidla (R-) atakuje tento elektrofilný uhlík. Zároveň sa dvojitá väzba C=O rozbije a elektróny sa presunú na atóm kyslíka, ktorý sa stane záporne nabitým (δ-). Týmto spôsobom sa vytvorí novo vzniknutý alkoxidový intermediát, kde je organická skupina z Grignardovho činidla naviazaná na pôvodný karbonylový uhlík, a horčíkový komplex je naviazaný na kyslík.
Po ukončení reakcie s karbonylovou zlúčeninou sa zvyčajne pridá vodný roztok kyseliny (napr. zriedená HCl alebo H2SO4). Táto kyslá hydrolýza rozbije horčíkový komplex a protonizuje alkoxidový kyslík, čím sa uvoľní výsledný alkohol. Vedľajším produktom je halogenid horečnatý (MgX2).
Syntéza terciárnych alkoholov
Syntéza terciárnych alkoholov pomocou Grignardových činidiel je obzvlášť významná, pretože tieto alkoholy často nie je možné ľahko získať inými metódami. Terciárny alkohol má tri organické skupiny naviazané na uhlík nesúci hydroxylovú skupinu.
Reakcia s ketónmi: Pri reakcii Grignardovho činidla s ketónom (R'COR'') vzniká po hydrolýze terciárny alkohol. V tomto prípade sa na karbonylový uhlík pripoja dve organické skupiny z ketónu (R' a R'') a jedna organická skupina (R) z Grignardovho činidla. Všeobecný vzorec takto pripraveného terciárneho alkoholu je RR'R''C-OH.
Príkladom môže byť reakcia metylmagnéziumbromidu (CH3MgBr) s acetónom ((CH3)2CO). Po hydrolýze vznikne 2-metyl-2-propanol (tert-butanol).
Reakcia s estermi: Grignardove činidlá môžu reagovať aj s esterami. Reakcia s esterom je však zložitejšia, pretože Grignardovo činidlo môže reagovať dvakrát. Prvá molekula Grignardovho činidla atakuje karbonylový uhlík esteru, pričom sa odštiepi alkoxidová skupina esteru. Vzniká ketón. Tento novovzniknutý ketón je však stále reaktívny voči ďalšej molekule Grignardovho činidla. Druhá molekula Grignardovho činidla atakuje ketón, čím po hydrolýze opäť vzniká terciárny alkohol. V tomto prípade sú dve z troch organických skupín naviazaných na uhlík nesúci hydroxylovú skupinu rovnaké (pochádzajúce z druhej molekuly Grignardovho činidla), zatiaľ čo tretia skupina pochádza z pôvodnej organickej časti esteru.
Príkladom je reakcia fenylmagnéziumbromidu (PhMgBr) s metylacetátom (CH3COOCH3). Po reakcii s dvoma molekulami PhMgBr a následnej hydrolýze vznikne 1,1-difenyl-1-etanol.
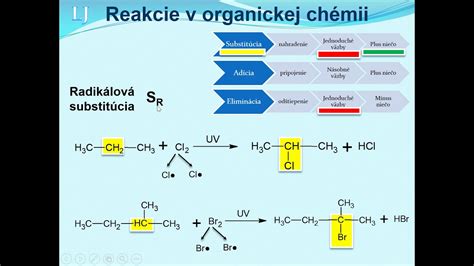
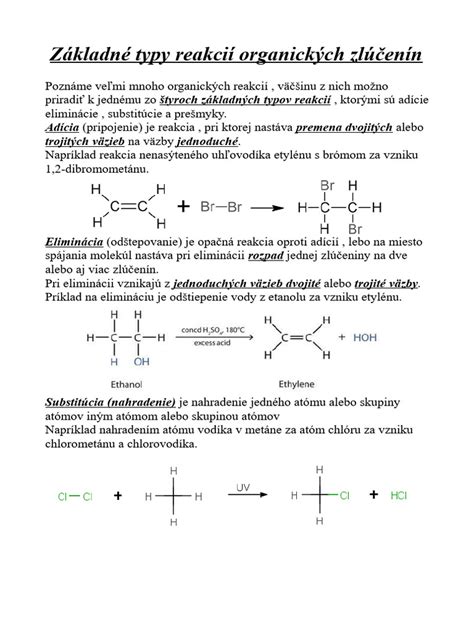
Reakcia s inými zlúčeninami: Grignardove činidlá môžu reagovať aj s inými zlúčeninami obsahujúcimi elektrofilné centrá, ako sú epoxidy (cyklické étery), ktoré po otvorení cyklu a následnej hydrolýze vedú k vzniku iných typov alkoholov. V prípade reakcie s epoxidmi sa predĺži uhlíkový reťazec a vznikne primárny alkohol.
Význam a aplikácie Grignardových činidiel
Grignardove činidlá sú nesmierne univerzálne a nachádzajú široké uplatnenie v organickej syntéze, od laboratórneho výskumu až po priemyselnú výrobu. Ich schopnosť tvoriť nové väzby uhlík-uhlík umožňuje konštrukciu komplexných molekulárnych štruktúr. Syntéza terciárnych alkoholov je len jednou z mnohých možností. Tieto alkoholy sú často dôležitými medziproduktmi pri výrobe liečiv, parfumov, polymérov a iných špecializovaných chemikálií.
Napriek svojej reaktivite a citlivosti na vlhkosť, s náležitou opatrnosťou a dodržiavaním bezpečnostných protokolov, sú Grignardove činidlá nenahraditeľným nástrojom pre chemikov po celom svete. Ich objav znamenal zásadný pokrok v organickej chémii a ich význam pretrváva dodnes.
Historický kontext objavu Grignardových činidiel je fascinujúci. François Auguste Victor Grignard pôvodne študoval matematiku, ale neskôr sa preorientoval na chémiu. Jeho objav organohorečnatých zlúčenín v roku 1901 a následné rozpracovanie ich syntetického potenciálu mu priniesli Nobelovu cenu za chémiu v roku 1912. Jeho práca otvorila dvere k mnohým novým syntetickým cestám, ktoré boli predtým nepredstaviteľné.
Je dôležité poznamenať, že Grignardove činidlá reagujú nielen ako nukleofily, ale aj ako silné bázy. S protickými substrátmi, ako sú alkohol, voda alebo karboxylové kyseliny, reagujú ako bázy, pričom odštiepujú protón a tvoria príslušný alkoxid alebo inú soľ horčíka. Tieto reakcie často vyžadujú následné spracovanie vodou, ktoré sa v reakčných schémach niekedy neuvádza.
V oblastiach ako farmaceutický priemysel, kde je presná syntéza komplexných molekúl nevyhnutná, sa Grignardove reakcie používajú na výrobu účinných látok. Napríklad, syntéza určitých liekov proti rakovine alebo iných bioaktívnych molekúl môže zahŕňať kroky využívajúce Grignardove činidlá na vytvorenie kľúčových uhlík-uhlíkových väzieb. Ich schopnosť reagovať selektívne s rôznymi funkčnými skupinami, najmä v prítomnosti vhodných katalyzátorov, ich robí mimoriadne cennými. Napríklad, v couplingových reakciách s organickými halogenidmi v prítomnosti katalyzátorov na báze železa alebo niklu sa dajú vytvoriť nové uhlík-uhlíkové väzby medzi dvoma organickými fragmentami.
Vedecký pokrok v oblasti Grignardových činidiel pokračuje aj v súčasnosti. Výskum sa zameriava na vývoj nových metód ich prípravy, na rozšírenie ich reaktivity a na zlepšenie selektivity reakcií. Zvláštny dôraz sa kladie na metódy, ktoré sú šetrnejšie k životnému prostrediu a umožňujú efektívnejšie využitie zdrojov. Napríklad, vývoj katalytických systémov, ktoré umožňujú použitie menšieho množstva Grignardovho činidla alebo pracujú za miernejších podmienok, je aktívnou oblasťou výskumu. Okrem toho sa skúmajú aj nové aplikácie v oblasti materiálových vied a supramolekulárnej chémie.
tags: #grinardove #cinidlo #a #terciarny #alkohol