Pri pojme "alkohol" si určite najskôr vybavíte nápoj. V chémii sú však alkoholy oveľa viac ako len spoločenské “mazivo”. Sú to fascinujúce organické zlúčeniny, ktoré tvoria základ mnohých chemických procesov a nachádzajú uplatnenie v širokom spektre odvetví. V tejto komplexnej príručke sa ponoríme do sveta alkoholov, preskúmame ich štruktúru, vlastnosti a predovšetkým to, ktoré z nich sa môžu premeniť na kyseliny, a ako k tejto premene dochádza.
Základy alkoholov: Štruktúra a klasifikácia
Alkoholy v chémii tvoria skupinu organických zlúčenín, ktoré obsahujú jednu alebo viac hydroxylových (-OH) funkčných skupín pripojených k atómu uhlíka. Sú významnou súčasťou organickej chémie a ich štúdium ponúka hlbšie porozumenie tejto problematike. Všeobecný vzorec pre alkohol je R-OH, kde R predstavuje akúkoľvek alkylovú skupinu a -OH je hydroxylová skupina. Táto skupina je zodpovedná za charakteristické vlastnosti a reakcie, ktoré vykazujú alkoholy.
Molekula alkoholu je polárna vďaka rozdielu elektronegativity medzi atómami kyslíka a vodíka v hydroxylovej skupine. Táto polarita spôsobuje, že alkoholy majú vyššie teploty varu ako iné organické zlúčeniny podobnej veľkosti. Vďaka všestrannosti a reaktivite molekuly alkoholu ide o základnú súčasť organickej chémie.
Alkoholy sa delia podľa počtu hydroxylových substituentov:
- Monohydroxidové alkoholy (monohydroxylové): Obsahujú jednu hydroxylovú skupinu.
- Polyhydroxidové alkoholy (polyhydroxyl): Obsahujú dve alebo viac hydroxylových skupín. Medzi nimi rozlišujeme v závislosti od počtu -OH skupín tzv. dioly, trioly atď.
Alkoholy sa tiež klasifikujú podľa poradia reakcie atómu uhlíka, ku ktorému je pripojená hydroxylová skupina (-OH):
- Primárne alkoholy: Atóm uhlíka pripojený k skupine -OH je spojený len s jedným ďalším atómom uhlíka. Príkladom je etanol.
- Sekundárne alkoholy: Atóm uhlíka pripojený k skupine -OH je spojený s dvoma ďalšími atómami uhlíka.
- Terciárne alkoholy: Atóm uhlíka pripojený k skupine -OH je spojený s tromi ďalšími atómami uhlíka.
Primárne alkoholy sú vďaka svojej reaktivite nevyhnutnou súčasťou mnohých chemických reakcií. Možno ich oxidovať za vzniku aldehydov a ďalej oxidovať za vzniku karboxylových kyselín. Táto vlastnosť sa využíva v rôznych chemických reakciách a je základom pri výrobe niektorých chemických látok. Pochopiť podstatu primárnych alkoholov je kľúčové pre každého, kto sa usiluje hlbšie porozumieť organickej chémii.
Kľúčové alkoholy a ich premieňanie na kyseliny
Nie všetky alkoholy sa však ľahko premieňajú na kyseliny, a dokonca ani nie všetky alkoholy sú bezpečné pre ľudskú spotrebu. Je veľmi dôležité poznať rôzne druhy alkoholov a ich vlastnosti.
Metanol (CH₃OH) - Metylalkohol
Metanol, tiež známy ako metylalkohol, je najjednoduchší alkohol. Je to bezfarebná, prchavá a veľmi jedovatá látka. 50 cm³ metanolu spôsobuje smrť. Využíva sa ako rozpúšťadlo olejov, má dezinfekčné účinky, je súčasťou čistiacich prostriedkov a slúži ako východisková surovina pri výrobe kyselín. Pri výrobe sa často používa ako katalyzátor kyselina trihydrogenfosforečná na oxide kremičitom. Vzniká tiež oxidáciou metanolu.
Premena na kyselinu: Metanol sa môže oxidáciou premeniť na formaldehyd (metanal) a následne na kyselinu mravčiu (kyselinu metánovú). Formaldehyd (CH₃CHO) je bezfarebný, štipľavo zapáchajúci, jedovatý plyn, ktorý vzniká oxidáciou metanolu. Používa sa na výrobu plastov, ako dezinfekčný prostriedok a konzervačná látka biologických preparátov.
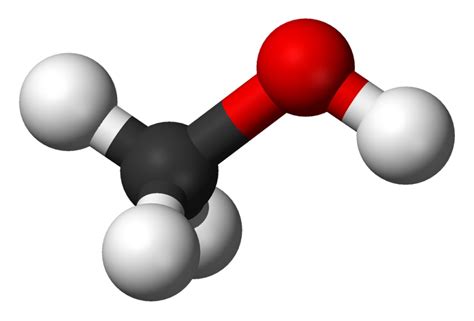
Etanol (C₂H₅OH) - Etylalkohol
Etanol, známy aj ako etylalkohol alebo lieh, je alkohol, ktorý sa nachádza v alkoholických nápojoch. Ide o primárny alkohol, ktorý je v miernom množstve bezpečný pre ľudskú spotrebu. Etanol je bezfarebná, horľavá kvapalina s charakteristickým zápachom, patriaca medzi silné narkotiká. Jeho požitie najprv vyvoláva povzbudenie a neskôr paralýzu nervového systému. Má teplotu varu 78 °C.
Premena na kyselinu: Etanol sa môže oxidáciou premeniť na acetaldehyd (etanal) a ďalej na kyselinu octovú (kyselinu etánovú). Acetaldehyd (C₂H₅OH) je prchavá, jedovatá látka s teplotou varu 28 °C. Vzniká pri travení alkoholu. Kyselina octová je známa svojimi konzervačnými účinkami (2% - 3% roztok), ničí baktérie a plesne. 100% kyselina octová tuhne pri 17 °C a mieša sa s vodou v každom pomere. Pary kyseliny octovej sú horľavé. Soli kyseliny octovej sa nazývajú octany.
Premena etanolu na kyselinu octovú prebieha tiež pôsobením mikroorganizmov, hlavne rodu Acetobacter (tzv. octové kvasenie, napr. pri výrobe octu z vína). Priama reakcia s kyslíkom môže prebiehať ako horenie, pri ktorom sa etanol oxiduje až na oxid uhličitý a vodu.
Oxidácia etanolu na kyselinu etánovú pomocou permaganátu draselného
Glycerol (Propán-1,2,3-triol)
Glycerol, tiež známy ako glycerín, je zložkou tukov a olejov, z ktorých sa ziskava. Je to trojsýtny alkohol (má tri hydroxylové skupiny). Je to bezfarebná, bez zápachu, ale sladkej chuti, hygroskopická kvapalina. V medicíne, kozmetickom a potravinárskom priemysle sa používa ako zvlhčovadlo, zmäkčovadlo a sladidlo. Nachádza uplatnenie aj pri výrobe pečiarkových a tlačiarenských farieb a výbušnín (nitráciou vzniká nitroglycerín). Vzniká ako vedľajší produkt kvasenia glukózy (na úkor etanolu) alebo ako vedľajší produkt pri zmydelňovaní tukov.
Premena na kyselinu: Glycerol samotný sa priamo nepremieňa na bežné karboxylové kyseliny v zmysle oxidácie hydroxylových skupín na karboxylové. Jeho štruktúra umožňuje iné typy reakcií, napríklad dehydratáciou môže vzniknúť akroleín. Hoci nie je priamym prekurzorom v tomto zmysle, jeho estery (tuky) sa môžu hydrolýzou rozkladať na glycerol a mastné kyseliny.
Acetaldehyd (Etanal) a Formaldehyd (Metanal)
Acetaldehyd (C₂H₅OH, etanal) je prchavá jedovatá látka s teplotou varu 28 °C. Vzniká pri travení alkoholu a používa sa pri výrobe liečiv, kaučuku a kyselín.Formaldehyd (CH₃CHO, metanal) vzniká oxidáciou metanolu. Je to bezfarebný, štipľavo zapáchajúci jedovatý plyn, používaný na výrobu plastov a ako dezinfekčný prostriedok či konzervačná látka.
Premena na kyselinu: Tieto látky sú už medziproduktami v procese oxidácie alkoholov. Acetaldehyd sa môže ďalej oxidovať na kyselinu octovú a formaldehyd na kyselinu mravčiu.
Aceton (Dimetylketón)
Aceton (CH₃COCH₃) je významné rozpúšťadlo pre farby, laky a čistiace prostriedky. Má teplotu varu 56 °C a intenzívne sa vyparuje, pričom môže mať narkotické účinky a poškodzovať centrálny nervový systém. Aceton je ketón, nie alkohol, a preto sa sám priamo neoxiduje na karboxylové kyseliny v bežnom zmysle, hoci sa môže podieľať na iných chemických reakciách.
Kyseliny priamo z prírody a ich vlastnosti
Niektoré kyseliny, ktoré sa spomínajú v súvislosti s alkoholmi, sa vyskytujú aj priamo v prírode alebo vznikajú v dôsledku metabolických procesov.
Kyselina mravčia (HCOOH) - Kyselina metánová
Kyselina mravčia je bezfarebná kvapalina so silným zápachom a leptavými účinkami. Obsahujú ju mravce (až 20% hmotnosti), včely a osy. Je veľmi silná a má dezinfekčné účinky - ničí baktérie a plesne. Používa sa na odstraňovanie vodného kameňa a má konzervačné účinky (napr. v ovocných šťavách). Vzniká oxidáciou metanolu.
Kyselina octová (CH₃COOH) - Kyselina etánová
Kyselina octová je známa ako hlavná zložka octu. Mieša sa s vodou v každom pomere. 100% kyselina octová tuhne pri 17 °C. V koncentrácii 2%-3% má konzervačné účinky, ničí baktérie. 8% roztok je bežný potravinársky ocot. Je silno leptavá a jej pary sú horľavé. Používa sa na konzerváciu, odstraňovanie vodného kameňa, pri výrobe umelej hodvábu a liečiv. Soli kyseliny octovej sú octany. Vzniká oxidáciou etanolu.
Kyselina maslová (C₃H₇COOH) - Kyselina butánová
Kyselina maslová vzniká kvasením škrobov (cukrov) a rozkladom masla. Nachádza sa aj v pote cicavcov. Má charakteristický, pre mnohých nepríjemný zápach.
Kyselina šťaveľová (HOOC-COOH) - Kyselina etándiolová
Kyselina šťaveľová sa vyskytuje napríklad v šťavele a rebarbore.
Reakcie alkoholov: Viac než len oxidácia
Alkoholy sa nezúčastňujú len oxidačných reakcií vedúcich k tvorbe kyselín. Ich hydroxylová skupina (-OH) im dodáva širokú škálu reaktivity.
- Esterifikácia: Esterifikácia je kyselinou katalyzovaná reakcia alkoholu s kyselinou alebo jej derivátom za vzniku esteru a vody. Napríklad reakciou etanolu s kyselinou octovou vzniká etylacetát (ester) a voda. Tento proces je kľúčový pri výrobe vonných a aromatických látok.
- Dehydratácia: V prítomnosti kyseliny sa alkoholy môžu dehydrovať za vzniku alkénov. Zjednodušený vzorec je R-OH → R=CH₂ + H₂O.
- Reakcia s alkalickými kovmi: Etanol búrlivo reaguje s alkalickými kovmi (napr. sodíkom), pričom vzniká unikajúci vodík a etoxid sodný.
Význam a využitie alkoholov
Alkoholy hrajú v chémii významnú úlohu. Podieľajú sa na rôznych reakciách a používajú sa ako rozpúšťadlá.
- Rozpúšťadlá: Alkoholy ako etanol slúžia ako univerzálne rozpúšťadlá v laboratóriách a priemysle vďaka svojej schopnosti rozpúšťať polárne aj nepolárne látky. Etanol je relatívne bezpečný a možno ho použiť na rozpustenie mnohých zlúčenín nerozpustných vo vode. Metanol je ďalším populárnym rozpúšťadlom, používaným predovšetkým pri syntéze iných chemikálií.
- Výroba biopalív: Etanol sa používa na výrobu biopalív, obnoviteľných zdrojov energie. Je to vysoko hodnotné ekologické palivo pre spaľovacie motory s antidetonačnými vlastnosťami.
- Antiseptiká a dezinfekcia: Etanol sa vďaka svojej schopnosti ničiť mikroorganizmy používa ako antiseptikum a na dezinfekciu neporanenej kože.
- Priemyselné využitie: Alkoholy sa používajú pri výrobe plastov, liečiv, kozmetiky (parfumy), čistiacich prostriedkov, nemrznúcich zmesí, atramentov a mnohých ďalších produktov. Glycerol sa používa v medicíne, kozmetike a potravinárstve.
Bezpečnosť a zodpovedné používanie
Hoci sú alkoholy všestranné a užitočné, môže byť ťažké zabezpečiť ich bezpečné používanie. Sú to nebezpečné zlúčeniny, ktoré si vyžadujú osobitnú opatrnosť.
- Toxicita: Nie všetky alkoholy sú bezpečné na konzumáciu. Metanol je napríklad vysoko toxický a jeho požitie môže viesť k vážnym zdravotným problémom, vrátane oslepnutia a smrti. Etanol je v miernom množstve bezpečný, ale jeho nadmerná konzumácia poškodzuje centrálny nervový systém. Etanol sa zvyčajne denaturuje (doslova pozbavuje prirodzených vlastností) metanolom alebo inými toxickými látkami pri predaji na technické účely, aby sa obišla spotrebná daň.
- Skladovanie a manipulácia: Alkoholy ako suroviny, medziprodukty a produkty by mali mať primeranú kvalitu a je zakázané používať a predávať kontaminovaný tovar. Od syntézy až po odoslanie spotrebiteľovi sa musia správne skladovať, aby sa vylúčilo riziko kontaminácie alebo úniku počas prepravy. Faktory ako správna teplota alebo blízkosť iných chemikálií môžu mať významný vplyv na bezpečnosť.
- Odpadové hospodárstvo: Odpad vznikajúci pri výrobe, priemyselnom spracovaní alebo individuálnom použití podlieha zneškodňovaniu. Odporúča sa kontaktovať spoločnosti, ktoré sa špecializujú na bezpečnú likvidáciu chemického odpadu.
Pochopenie etanolu a jeho úlohy ako primárneho alkoholu v chémii je kľúčové pre každého, kto chce porozumieť svetu alkoholov. Vďaka jeho jedinečným vlastnostiam a všestrannosti ide o základnú zlúčeninu v rôznych chemických reakciách a procesoch. Cesta k ich pochopeniu je skutočne obohacujúca.