Voda, základná zložka života na Zemi, je objektom neustáleho záujmu nielen pre jej biologický význam, ale aj pre jej fascinujúce fyzikálne vlastnosti. Jednou z najzákladnejších vlastností, s ktorou sa stretávame už v škole, je jej bod varu, tradične udávaný ako 100 °C. Experimentálne však často zistíme, že nameraná teplota varu vody nie je presne 100 °C, ale skôr menej. Tento jav, spolu s ďalšími vlastnosťami vody, otvára dvere k hlbšiemu pochopeniu jej správania a významu v rôznych procesoch.

Pochopenie bodu varu: Viac ako len teplota
Teplota varu kvapaliny je definovaná ako teplota, pri ktorej sa tlak pár nad povrchom kvapaliny rovná tlaku okolia. V prípade vody je táto hodnota 100 °C za štandardného atmosférického tlaku 101,3 kPa (kilopascalov). Je však dôležité si uvedomiť, že tento údaj je ideálny a v praxi sa môžu vyskytnúť odchýlky.
Prvá vec, ktorá obvykle upúta pozornosť študentov pri experimentálnom meraní teploty varu vody, je fakt, že nameraná teplota nie je presne 100 °C, ale býva nižšia. Častú argumentáciu študentov, že ide iba o nepresnosť teplotného čidla, je možné oslabiť alebo priamo vyvrátiť použitím dvoch či viacerých rôznych teplomerov súčasne. Ak chceme študentom pomôcť v riešení tejto "záhady", môžeme im naznačiť, že 100 °C je teplota varu vody za normálneho atmosférického tlaku. S touto indíciou študenti obyčajne dospejú k záveru, že teplota varu vody závisí od tlaku vzduchu.
Atmosférický tlak a bod varu
Vplyv tlaku na bod varu je jedným z kľúčových faktorov, ktoré ovplyvňujú, kedy voda začne vrieť. Tento tlak nie je len teoretický koncept; je ovplyvnený napríklad aktuálnym stavom počasia, ktoré mení atmosférický tlak, alebo nadmorskou výškou, v ktorej sa experimentátor nachádza. Napríklad, ak je tlak vzduchu prepočítaný na hladinu mora práve tých "normálnych" 101,3 kPa, v nadmorskej výške 300 metrov nad morom bude tlak mierne nižší, čo povedie k mierne nižšej teplote varu vody. Tento jav je zásadný pre pochopenie variability bodu varu v rôznych geografických lokalitách.
Tlakový hrniec je praktickým príkladom využitia tejto závislosti. V ňom sa vďaka zvýšenému tlaku v uzavretom priestore varí kvapalina pri vyššej teplote, ako v otvorenej nádobe. Toto umožňuje rýchlejšie varenie jedál. Naopak, vo vákuových nádobách, z ktorých sa odsáva para, vrie kvapalina pri nižšej teplote ako pri normálnom tlaku.
Voda: Viac ako len H2O
Voda, chemicky známa ako oxid vodný s molekulárnym vzorcom H2O, je základnou chemickou zlúčeninou vodíka a kyslíka. Je to biologicky najdôležitejšie polárne rozpúšťadlo a najrozšírenejšia zlúčenina na Zemi, pokrývajúca približne 70,7 % zemského povrchu. Jej prítomnosť je nevyhnutná pre všetky živé organizmy. V živých organizmoch voda tvorí viac ako polovicu (cca 60-99 %) ich objemu, v závislosti od druhu.
Voda hrá kritickú úlohu v mnohých biologických procesoch: podieľa sa na termoregulácii, prenose látok, udržiavaní pH rovnováhy, odstraňovaní odpadových produktov metabolizmu a slúži ako reakčné prostredie pre biochemické reakcie.
Fyzikálne vlastnosti vody: Od hustoty po elektrickú vodivosť
Voda je v bežných podmienkach bezfarebná, číra kvapalina bez chuti a zápachu. Jej bod topenia je 0 °C a bod varu je 100 °C pri normálnom atmosférickom tlaku, čo sú hodnoty, z ktorých vychádza Celsiova teplotná stupnica.
Anomália vody: Jednou z najzaujímavejších vlastností vody je jej anomálne správanie, týkajúce sa hustoty. Hustota vody sa od 0 °C do 3,98 °C zvyšuje, pričom maximálnu hustotu (1 g/cm³) dosahuje práve pri 3,98 °C. S rastúcou teplotou nad touto hodnotou hustota klesá. Pri ochladzovaní pod 3,98 °C dochádza opäť k poklesu hustoty, nepriamo úmerne so zväčšujúcim sa objemom. Tento jav je dôvodom, prečo ľad pláva na vode - má menšiu hustotu ako kvapalná voda. Na rozdiel od väčšiny bežných látok, pri ktorých sa objem so zvyšujúcou teplotou zväčšuje a so znižujúcou sa teplotou zmenšuje vo všetkých teplotných intervaloch, voda sa správa odlišne. Anomália vody má zásadný význam pre vodný život, pretože vrstva ľadu tvoriaca sa na povrchu vodných plôch bráni hlbšiemu premŕzaniu vodných nádrží, čím chráni vodné organizmy pred uhynutím. Pri topení ľad zmenšuje svoj objem, pri tuhnutí ho zväčšuje. Kvantitatívne, relatívne zväčšenie objemu pri prechode z kvapalného skupenstva na pevné je približne 9 %.
Viskozita: Viskozita vody klesá so zvyšujúcou sa teplotou. Táto vlastnosť je dôležitá napríklad pri odvodňovaní vôd pieskom alebo pri sedimentácii v čističkách odpadových vôd, kde rýchlosť filtrácie a sedimentácie závisí od viskozity vody.
Povrchové napätie: Povrchové napätie vody taktiež klesá so zvyšujúcou sa teplotou. Voda má druhé najvyššie povrchové napätie spomedzi bežných látok, čo je dôležité pre kapilárne javy, napríklad pri vzlínaní vody v pôde alebo v rastlinách. Chemické pracie prostriedky toto povrchové napätie znižujú, čím uľahčujú pranie.
Tepelná vodivosť: Voda má veľmi malú tepelnú vodivosť. Táto vlastnosť zabraňuje rýchlemu zamŕzaniu vodných plôch do veľkých hĺbok, čo opäť prispieva k ochrane vodného života.
Elektrická vodivosť: Elektrická vodivosť vody je priamo závislá od obsahu rozpustených iónov. Čistá voda je veľmi slabým vodičom elektrického prúdu. Pridanie iónov, napríklad solí, výrazne zvyšuje jej elektrickú vodivosť. Tento princíp sa využíva napríklad pri meraní kvality vody.
Merná tepelná kapacita: Voda má pomerne vysokú mernú tepelnú kapacitu, približne 4184 J⋅kg−1⋅K−1 pri 20 °C. To znamená, že na ohriatie alebo ochladenie určitého množstva vody je potrené značné množstvo energie. Tento jav sa využíva napríklad v systémoch ústredného vykurovania, kde voda slúži ako médium na prenos tepla.
Voda ako rozpúšťadlo a jej reaktivita
Voda je univerzálnym rozpúšťadlom vďaka svojej polarite. Molekula vody má tvar mierne skoseného štvorstena s uhlom medzi vodíkovými väzbami približne 105°. Táto konfigurácia je daná dvoma voľnými elektrónovými pármi na atóme kyslíka. Kyslík nesie čiastočný záporný náboj (parciálny záporný náboj), zatiaľ čo vodíky nesú čiastočný kladný náboj. Táto nerovnomerná distribúcia elektrónovej hustoty medzi vodíkom a kyslíkom je spôsobená rozdielnou elektronegativitou atómov. Prítomnosť vodíkov umožňuje tvorbu vodíkových mostíkov medzi molekulami vody, ktoré zásadne ovplyvňujú jej fyzikálne a chemické vlastnosti, vrátane polarity, bodu topenia, bodu varu a skupenstva. Celá molekula vody je polárna vďaka polarite väzieb a dipólovému momentu.
V prírode sa voda takmer nikdy nevyskytuje v absolútne čistej forme. Zvyčajne obsahuje rôzne množstvo rozpustených látok. Hydráty sú kryštalické látky, ktoré obsahujú viazané molekuly vody, napríklad modrá, biela alebo zelená skalica. Destilovaná voda má pH 7, čo značí neutrálnu reakciu. pH vody sa mení v závislosti od rozpustených látok.
Tvrdosť vody, spôsobená rozpustnými soľami vápnika a horčíka, je častou prekážkou v bežnom používaní vody. Rozlišujeme dva typy tvrdosti: prechodnú (uhličitanovú) a trvalú (neuhličitanovú), pričom trvalá tvrdosť je spôsobená hlavne síranmi a chloridmi.
Napriek svojej univerzálnosti ako rozpúšťadlo je voda z hľadiska reaktivity jednou z najstabilnejších zlúčenín. Rozkladá sa na vodík a kyslík až pri vysokých teplotách.
Voda v rôznych skupenstvách a na rôznych telesách
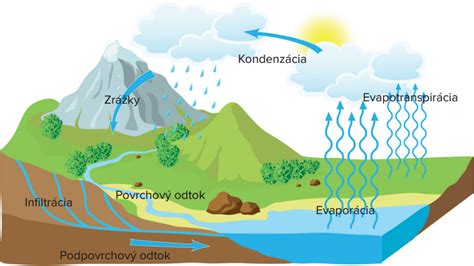
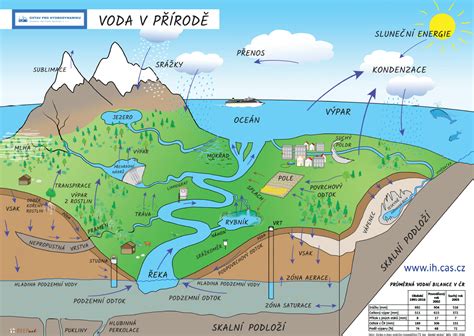
Voda sa na Zemi vyskytuje vo všetkých troch skupenstvách. V kvapalnom skupenstve sa nachádza v oceánoch, moriach, jazerách, riekach a potokoch. V pevnom skupenstve (ľad a sneh) sa vyskytuje vo vysokých nadmorských výškach a pokrýva rozsiahle oblasti pólarných oblastí, ako je Antarktída a Arktída. V plynnom skupenstve (vodná para) je neoddeliteľnou súčasťou atmosféry a hrá kľúčovú úlohu v kolobehu vody.
Zaujímavé je, že voda sa vyskytuje aj na iných telesách slnečnej sústavy. Na Marse sa dnes nachádza iba vo forme ľadu na južnom póle. Na Jupiteri a Saturne sa voda vyskytuje v nepatrnom množstve v atmosfére alebo pod povrchom. Jupiterov mesiac Európa je kamenná guľa pokrytá ľadom. Saturn má hustotu nižšiu ako voda. Urán a Neptún, napriek svojej veľkosti, majú nižšiu hustotu ako Zem a sú tvorené hlavne zmesou vodného, metánového a čpavkového ľadu. Aj na Plute, bývalej planéte, sa voda v tuhom skupenstve vyskytuje vo veľkom množstve. Venuša má naopak extrémne hustú atmosféru, ktorá spôsobuje teploty vysoko nad bodom varu vody.
Nedávno bol objavený aj štvrtý stav vody, ktorý vykazuje známky kvantového systému. Vyskytuje sa v extrémne malých kanálikoch minerálu beryl a jeho podstata spočíva v schopnosti molekuly vody "pretunelovať" cez energetickú bariéru.
Voda v priemysle a technike
Voda zohráva kľúčovú úlohu v mnohých priemyselných procesoch. Jednoduchým odsoľovacím zariadením je destilačný prístroj, kde sa vodná para zohrievaním oddeľuje od rozpustených solí a následne kondenzuje. Moderné odsoľovacie systémy, založené na princípe reverznej osmózy s použitím špeciálnych membrán, sú oveľa efektívnejšie pri premene slanej vody na pitnú.
Voda sa však môže znehodnotiť rôznymi chemickými látkami, ropnými produktmi, ťažkými kovmi, rádioaktívnym odpadom či splaškovými vodami. Tieto znečistenia vyžadujú úpravu, najmä v prípade povrchovej vody určené na pitie. Proces úpravy vo vodárňach zahŕňa usadzovanie pevných látok, pridávanie chemických látok na tvorbu zrazenín a následnú filtráciu cez pieskové filtre.
V technických aplikáciách sa stretávame aj s problémom vodného kameňa, ktorý vzniká usadzovaním minerálov, najmä uhličitanov vápnika a horčíka. Tento vodný kameň znižuje energetickú účinnosť systémov, ako sú kotly a chladiace veže. Existujú špeciálne chemické prostriedky, ako napríklad KALK-X, ktoré nekorozívnym spôsobom odstraňujú vodný kameň a obnovujú optimálnu funkciu zariadení. Pri ich aplikácii je však dôležité dodržiavať bezpečnostné pokyny a správne dávkovanie.
Voda je teda oveľa viac než len jednoduchá kvapalina. Jej vlastnosti, od bodu varu až po jej anomálne správanie, sú fascinujúce a zásadné pre pochopenie sveta okolo nás, od biologických procesov až po technické aplikácie.
tags: #pociatocna #teplota #varu #a #destilacny #rozsah