Alkohol, ako široko používaná látka, má mnoho rozličných aplikácií, od výroby nápojov až po priemyselné procesy. V tomto článku sa zameriame na jeho spaľovacie vlastnosti, konkrétne na teplotu horenia rôznych druhov alkoholu, s dôrazom na etanol a metanol. Budeme sa zaoberať ich fyzikálnymi a chemickými vlastnosťami, procesmi ich výroby, ako aj bezpečnostnými aspektmi pri ich používaní.

Etanol: Všestranný alkohol
Etanol, známy aj ako etylalkohol alebo lieh, je bezfarebná horľavá kvapalina s charakteristickým zápachom. V chemickom zmysle ide o jednosýtny alkohol s molekulovým vzorcom C2H5OH. Jeho teplota vzplanutia je 12 °C a teplota samovznietenia 392 °C. Etanol je neobmedzene rozpustný vo vode, metanole, acetóne, éteri, chloroforme a iných organických rozpúšťadlách. Má teplotu varu 78,3 °C a hustotu 0,7893 g·cm⁻³.
Najväčšia časť produkcie etanolu sa pripravuje z jednoduchých sacharidov (cukrov) alkoholickým kvasením pôsobením rôznych druhov kvasiniek, predovšetkým rôznych šľachtených kmeňových druhov Saccharomyces cerevisiae. Používa sa na to ako cukrový roztok (o maximálnej koncentrácii 20 %), tak aj priamo prírodné suroviny obsahujúce sacharidy, ako sú napr. zemiaky alebo cukrová trstina. Kvasením vzniká zápara, čiže veľmi zriedený vodný roztok etanolu (maximálne 15 %). Táto zápara vždy obsahuje nežiaduce prímesi, ako sú vyššie alkoholy (propanol a izopropanol), viac sýtené alkoholy (glycerol), ketóny (acetón) a iné.
Čistenie získaného etanolu sa uskutočňuje na výkonných destilačných kolónach. Možno získať tzv. azeotropný alkohol, obsahujúci 95,57 % etanolu a 4,43 % vody. Zvyšok vody možno odstrániť destiláciou s bezvodným síranom vápenatým alebo oxidom vápenatým, ktoré vodu viažu, alebo dlhodobým pôsobením hygroskopických látok ako napr. bezvodného uhličitanu draselného alebo bezvodného síranu meďnatého (modrej skalice), prípadne molekulových sít. Týmito postupmi možno získať etanol o čistote až 99,9 % (tzv. absolútny alkohol alebo bezvodý etanol, obsahujúci menej než 0,5 % vody a viac než 99,5 % etanolu).
Samotný etanol je látka pomerne reaktívna. Zvlášť búrlivo reaguje s alkalickými kovmi (sodíkom alebo draslíkom), pričom produktom tejto reakcie je unikajúci vodík a etoxid sodný (etanolát sodný). Pôsobením oxidačných činidiel dochádza k jeho oxidácii. Premena etanolu na kyselinu octovú prebieha tiež pôsobením mikroorganizmov, hlavne rodu Acetobacter (tzv. octové kvasenie, napr. pri výrobe octu z vína). Priama reakcia s kyslíkom môže prebiehať ako horenie, pri ktorom sa etanol oxiduje až na oxid uhličitý a vodu.
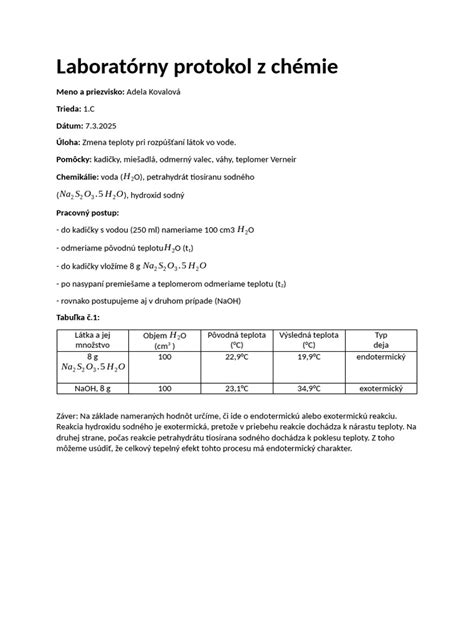
Priama reakcia s kyslíkom pri horení je kľúčovým aspektom našej témy. Hoci etanol horí v bežných podmienkach, jeho plameň má nažltlé konce. Spomedzi sledovaných alkoholov (metanol, etanol, n-butanol) horí etanol stredne svietivým plameňom. Obecne platí, že teplota plameňa vznikajúceho horením alkoholov klesá s počtom uhlíkov v ich molekule. Čím je teplota nižšia, tým je plameň lepšie viditeľný okom.
Najznámejším použitím etanolu je výroba alkoholických nápojov. Na výrobu kvalitných destilátov (whisky, slivovica, calvados, jablkovica, hruškovica a iné) sa uprednostňuje dvojstupňová destilácia, kde obsah etanolu nebýva vyšší ako 70 %. Etanol sa tiež používa pre zlepšenie výkonu spaľovacích motorov ako prídavok do pohonných hmôt. V medicíne sa používa ako rozpúšťadlo (napr. jódu, čím vzniká tzv. jódová tinktúra), pri príprave niektorých kvapalných prípravkov pre vnútorné a vonkajšie použitie a k dezinfekcii neporanenej kože. V oblasti kozmetiky sa uplatňuje pri výrobe voňaviek. Tento alkohol má svoje miesto aj pri výrobe čistiacich prostriedkov.
Etanol je vysoko hodnotné ekologické palivo pre spaľovacie motory s antidetonačnými vlastnosťami. Etanol určený pre iné použitie ako na priamu konzumáciu, príp. na výrobu alkoholických nápojov, sa denaturuje (zbavuje sa prirodzených vlastností). Dôvodom sú ekonomicko-právne aspekty: na konzumný etanol je na Slovensku uvalená vysoká spotrebná daň. Preto sa do etanolu predávaného na technické účely pridávajú pre človeka toxické látky, aby sa obišla spotrebná daň. Etanol sa väčšinou denaturuje metanolom, benzínom, benzénom, izopropanolom, acetónom a inými látkami v závislosti na cieľovom použití.
Pri zmiešaní etanolu s vodou dochádza k tzv. kontrakcii, teda k zmenšeniu objemu a vývoju tepla. Najväčšia kontrakcia nastáva, ak sa zmieša 52 objemov liehu a 48 objemov vody. Tento roztok, bežne používaný na riedenie destilátov, má pri 20 °C len 96,3 objemov. Napríklad zmiešaním 50 litrov vody a 50 litrov etanolu nezískame 100 litrov, ale iba 96,4 litra zmesi o liehovitosti 51,87 % obj. Z toho vyplýva obtiažnosť merania objemu zmesi liehu a vody, teda destilátu nariedeného na určitú liehovitosť. Ak napríklad vyrobíte v pálenici 20 litrov destilátu o liehovitosti 65 % a nariedite ho ďalšími 5 litrami vody, nezískate 25 litrov destilátu, ale menej. Množstvo vyrobeného destilátu tak bude mať vždy menší objem, než je súčet jednotlivých zmiešaných zložiek.
3 Exp 1 Part 2 Density of Ethanol
Pre správne určenie množstva destilátu po zriedení je potrebné poznať jeho teplotu, objem pri danej teplote a koncentráciu pri danej teplote. Ak je teplota meraného liehu nižšia ako 20 °C, percento alkoholu sa pripočítava. Pri teplote nad 20 °C sa percento alkoholu naopak odčíta.
Metanol: Nebezpečný dvojník etanolu
Metanol, známy aj ako metylalkohol alebo karbinol, je najjednoduchší alifatický alkohol so sumárnym vzorcom CH3OH. Je to bezfarebná, alkoholicky zapáchajúca kvapalina, neobmedzene miešateľná s vodou. V porovnaní s etanolom má nižšiu teplotu varu (64,7 °C) a hustotu.
Metanol bol objavený v roku 1661 britským chemikom Robertom Boylom destiláciou dreva, odtiaľ jeho alternatívny názov drevný lieh. V roku 1834 francúzski vedci určili štruktúru jeho molekuly, čím sa zrodil koncept metylalkoholu. V súčasnosti sa metanol už nepre získava destiláciou dreva, ale hydrogenáciou oxidu uhoľnatého za prítomnosti katalyzátora.
Z ľudského hľadiska sú dve najdôležitejšie vlastnosti metanolu jeho vysoká toxicita a to, že je výborným rozpúšťadlom. Metanol nie je priamo toxický v zmysle okamžitého účinku, ale jeho metabolizmus v tele je extrémne nebezpečný. Už dávka 10 ml sa metabolizuje na kyselinu mravčiu, ktorá môže zničiť zrakový nerv a spôsobiť trvalú slepotu. Medzi ďalšie negatívne účinky expozície patrí hypoxia na bunkovej úrovni, metabolická acidóza a iné poruchy, ktoré môžu dokonca spôsobiť smrť. Za smrteľnú dávku sa považuje 15 ml čistého metanolu.
Prvá pomoc pri otrave metanolom spočíva vo vypití dvoch decilitrov kvalitného 40% alkoholu (napr. vodky) a okamžitom vyhľadaní lekárskej pomoci. Etanol spomalí rozklad metanolu v tele a poskytne tak čas na lekársky zásah. Je dôležité zdôrazniť, že zmiešanie etanolu s metanolom vo fľaši neutralizuje jedovatý účinok metanolu.

Metanol horí takmer bezfarebným plameňom. Methanol a ethanol sú vysoko horľavé kvapalné látky a sú tiež vysoko telivé látky vytvárajúce sa vzduchom výbušné zmesi s nízkou hodnotou dolnej medze výbuchu. Pred zahájením práce s týmito látkami je nevyhnutné zabezpečiť vhodné hasiace prostriedky (práškový hasiaci prístroj). Pri rozliatí použitých látok je potrebné ihneď zhasnúť plynové spotrebiče, vypnúť elektrický prúd a zabezpečiť dôkladné vetranie. Pre sanáciu je nutné použiť inertný sorpčný materiál.
Zamedziť kontaktu použitých látok s kožou a očami, nevdechovať ich výpary ani produkty horenia (dym). Zamedziť prieniku použitých látok do životného prostredia (nesmie sa dostať do kanalizácie). Je zakázané stierať kaluže rozliateho etanolu handrami z umelých vláken alebo plastovými stierkami - nebezpečenstvo vzniku statickej elektriny. V prípade požiaru nehaste vodou.
Pre chemický priemysel je metylalkohol dôležitou zložkou kľúčových reakcií. Vďaka ľahkej premene na formaldehyd, uhľovodíky a metylamín sa používa pri výrobe širokého spektra produktov každodennej potreby. Ročne sa celosvetovo vyrobí až 20 miliónov ton metanolu. Metanol sa používa vo farmakologickom priemysle, pri výrobe plastov a syntetických tkanín, ako aj farbív, fungicídov a dokonca aj fotografických filmov.
Porovnanie vlastností a teplôt horenia
Hoci metanol a etanol sú voľným okom nerozoznateľné a ich fyzikálne vlastnosti sa v mnohých aspektoch prekrývajú (bezfarebná kvapalina, charakteristický zápach, dobrá rozpustnosť vo vode), ich chemické vlastnosti a predovšetkým toxicita sa výrazne líšia. Tento zdanlivo malý rozdiel v chemickej štruktúre - jeden atóm uhlíka navyše v etanole - čiastočne mení vlastnosti etylalkoholu, vďaka čomu je pre ľudí bezpečnejší.
Pri laboratórnom pokuse s horením rôznych alkoholov (metanol, etanol, n-butanol) sa pozoruje rozdielne správanie. Páry metanolu a etanolu vo zmesi so vzduchom sa vznítia s miernym výbuchom, zatiaľ čo butanol sa vzníti až po chvíli zahrievania. Methanol horí takmer bezfarebným plameňom, konce plameňa horiaceho etanolu sú nažltlé a plameň horiaceho butanolu je žltý. Pozoruje sa tiež stúpajúca svietivosť plameňa v rade: metanol, etanol, n-butanol.
3 Exp 1 Part 2 Density of Ethanol
Ako už bolo spomenuté, obecne platí, že teplota plameňa vznikajúceho horením alkoholov klesá s počtom uhlíkov v jeho molekule. To znamená, že metanol, ako najjednoduchší alkohol, má potenciálne najvyššiu teplotu plameňa spomedzi týchto troch, hoci je ťažko vizuálne postrehnuteľná kvôli bezfarebnému plameňu. Etanol má o niečo nižšiu teplotu plameňa a horí žltším plameňom, čo naznačuje neúplné spaľovanie a prítomnosť uhlíkových častíc. Butanol, s ešte dlhším reťazcom, horí najžltším a najsvietivejším plameňom, čo svedčí o nižšej teplote plameňa.
Je dôležité dodržať na pracovnom mieste čistotu a poriadok. Odporúča sa prednostné použitie laboratórneho zapaľovača. Zapálenie horiacou špajdľou by mohlo spôsobiť vzplanutie pár alkoholov mimo porcelánovej misky. Zvyšok alkoholov môžeme nechať zhoreť alebo ich uložíme do uzatvorenej odpadovej nádoby s príslušným bezpečnostným označením a necháme zlikvidovať špecializovanou firmou.
Bezpečnostné aspekty a praktické využitie
Vzhľadom na ich horľavosť a potenciálnu toxicitu, najmä v prípade metanolu, je pri práci s alkoholmi nevyhnutné dodržiavať prísne bezpečnostné opatrenia. Je zakázané stierať kaluže rozliateho etanolu handrami z umelých vláken alebo plastovými stierkami kvôli nebezpečenstvu vzniku statickej elektriny. V prípade požiaru alkoholov nie je vhodné hasiť vodou.
Hoci etanol nie je toxický ako metanol, jeho konzumácia vo forme nápojov spôsobuje každoročne viac úmrtí. Je príčinou tragických dopravných nehôd, súvisí s ďalšími vážnymi zraneniami, samovraždami a ťažkými chorobami. Svetová zdravotnícka organizácia zaradila alkohol aj na zoznam karcinogénnych látok pre ľudí.
Metanol a etanol patria medzi kľúčové chemické suroviny v modernom svete. Okrem výroby alkoholických nápojov a liečiv je jednou z najdôležitejších oblastí použitia etanolu medicína, kde sa primárne používa na dezinfekciu a rozpúšťanie vo vode nerozpustných liečivých látok. Niekedy sa používa aj ako protijed pri otrave metanolom. Etanol sa používa aj pri výrobe automobilového a raketového paliva, palivových článkov, ako aj rozpúšťadiel, farieb, značkovačov a produktov osobnej starostlivosti. Umožňuje efektívnu extrakciu olejov z prírodných surovín, napr. konope. V laboratóriách sa používa na zníženie teploty používaných látok.
V krajinách, ktoré majú zdroje lacného fermentačného etanolu, sa používa na výrobu etylénu a ako zložka motorových palív. V súčasnosti sa takto používa aj v EÚ, v 95-oktánovom benzíne je ho 10 %. Etanol určený na technické účely sa niekedy zámerne znehodnocuje, aby sa zabránilo jeho konzumácii (denaturácia).