Alkoholy a aldehydy sú základné organické zlúčeniny, ktoré hrajú kľúčovú úlohu v chémii a majú široké spektrum využitia v priemysle aj v každodennom živote. Ich vzájomný vzťah je predovšetkým o transformáciách, kde jeden môže byť premenený na druhý prostredníctvom špecifických chemických reakcií. Pochopenie týchto procesov je nevyhnutné pre syntézu nových zlúčenín a pre optimalizáciu existujúcich výrobných postupov.
Klasifikácia a Štruktúra Alkoholov
Alkoholy sú organické zlúčeniny, ktoré obsahujú hydroxylovú funkčnú skupinu (-OH) viazanú na alifatický uhlíkový atóm. V závislosti od toho, na akom type uhlíka je -OH skupina naviazaná, rozlišujeme tri základné typy alkoholov:
- Primárne alkoholy: V nich je hydroxylová skupina viazaná na primárny uhlík, teda na uhlík, ktorý je spojený s jedným ďalším uhlíkovým atómom. Príkladom je etanol (C2H5OH), kde je -OH skupina viazaná na uhlík, ktorý je spojený len s jedným iným uhlíkom.
- Sekundárne alkoholy: V nich je hydroxylová skupina viazaná na sekundárny uhlík, teda na uhlík, ktorý je spojený s dvoma ďalšími uhlíkovými atómami. Typickým príkladom je izopropylalkohol (2-propanol), kde je -OH skupina na uhlíku, ktorý je spojený s dvoma metylovými skupinami.
- Terciárne alkoholy: V nich je hydroxylová skupina viazaná na terciárny uhlík, teda na uhlík, ktorý je spojený s tromi ďalšími uhlíkovými atómami.
Okrem tejto klasifikácie sa alkoholy delia aj podľa počtu hydroxylových skupín v molekule na:
- Nasýtené alkoholy: Obsahujú iba jednu hydroxylovú skupinu.
- Viacsýtné alkoholy (polyoly): Obsahujú viac ako jednu hydroxylovú skupinu. Tieto sú menej stabilné a majú tendenciu odštepovať molekuly vody.
Nízke alkoholy, ako metanol a etanol, sú za bežných podmienok kvapaliny s relatívne vysokým bodom varu. Táto vlastnosť je spôsobená prítomnosťou vodíkových väzieb medzi molekulami, ktoré si vyžadujú dodatočnú energiu na prekonanie pri prechode z kvapalného do plynného skupenstva.
Z chemického hľadiska vykazujú alkoholy mierne kyslý, ale aj mierne zásaditý charakter. Polarita väzby O-H, vyplývajúca z rozdielnej elektronegativity kyslíka a vodíka, im dodáva kyslé vlastnosti. Voči silným kyselinám sa však správajú ako zásady, pričom vznikajú alkoxóniové soli.
Reakcie Alkoholov: Dehydratácia a Dehydrogenácia
Alkoholy sú pomerne reaktívne zlúčeniny a podliehajú rôznym chemickým transformáciám. Dve kľúčové reakcie, ktoré súvisia s tvorbou aldehydov a iných organických zlúčenín, sú dehydratácia a dehydrogenácia.
Dehydratácia alkoholov je proces, pri ktorom dochádza k odštiepeniu molekuly vody. V závislosti od reakčných podmienok môžu vzniknúť alkány alebo étery. Táto reakcia vyžaduje prítomnosť vhodných katalyzátorov, ako je koncentrovaná sírová kyselina (H2SO4), pentoxid fosforu (P2O5), chlorid zinočnatý (ZnCl2), alebo sa dá uskutočniť vedením pár alkoholu cez kontaktný katalyzátor, napríklad oxid hlinitý (Al2O3), pri zvýšenej teplote. Dehydratácia prebieha najľahšie pri terciárnych alkoholoch a najťažšie pri primárnych. V procese dehydratácie platí Zajcevovo pravidlo, ktoré predpovedá, že v prípade vzniku viacerých možných produktov sa bude preferovať ten, ktorý má viac substituovaný dvojitú väzbu.
Dehydrogenácia alkoholov je proces, pri ktorom alkohol stráca dva atómy vodíka. Táto reakcia sa typicky uskutočňuje vedením pár alkoholu cez prehriaty kovový katalyzátor, najčastejšie meď alebo striebro. Kľúčovým výsledkom dehydrogenácie je transformácia primárneho alkoholu na aldehyd a sekundárneho alkoholu na ketón. Táto reakcia je základným krokom v syntéze mnohých aldehydov a ketónov.
Oxidácia Alkoholov: Cesta k Aldehydom a Karboxylovým Kyselinám
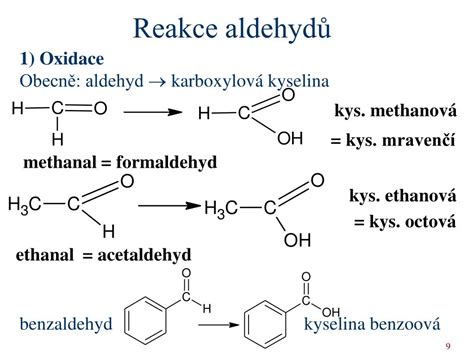
Oxidácia alkoholov je ďalšou zásadnou reakciou, ktorá priamo súvisí s tvorbou aldehydov. Použitím rôznych oxidačných činidiel, ako je kyselina chrómová (vytvorená z dichromanu draselného a kyseliny sírovej), dichromany alebo manganistany, je možné oxidovať alkoholy na rôzne produkty.
Primárne alkoholy sa pri miernej oxidácii premieňajú na aldehydy. Ak je však oxidačné činidlo dostatočne silné alebo reakcia prebieha dlhšie, aldehyd sa ďalej oxiduje na karboxylovú kyselinu. Napríklad, metanol (CH3OH) sa najprv oxiduje na formaldehyd (HCHO), ktorý sa ďalej môže oxidovať na kyselinu mravčiu (HCOOH), a pri silnejšej oxidácii sa rozkladá na vodu a oxid uhličitý (CO2).
Sekundárne alkoholy sa oxidujú priamo na ketóny. Ketóny sú menej reaktívne voči ďalšej oxidácii ako aldehydy.
Terciárne alkoholy sú voči oxidácii viac-menej odolné. Ich oxidácia si vyžaduje drastickejšie podmienky a zvyčajne vedie k štiepeniu uhlíkového reťazca.
Rozlišovanie medzi primárnymi a sekundárnymi alkoholmi sa často opiera o odlišné vlastnosti produktov ich oxidácie - aldehydov a ketónov. Aldehydy reagujú s tzv. Tollensovým, Fehlingovým alebo Benedictovým činidlom, pričom dochádza k ich redukcii.
Schiffovo Činidlo a Jeho Aplikácie
Schiffovo činidlo je špecifické činidlo používané na detekciu aldehydov. Je to vodný roztok fialovočerveného farbiva fuchsinu, ku ktorému sa pridáva hydrogensiřičitan alebo siřičitan. V kyslom prostredí sa hydrogensiřičitan aduje na centrálnu uhlíkovú väzbu farbiva, čím sa naruší jeho chinoidná štruktúra zodpovedná za sfarbenie, a vzniká bezfarebný roztok kyseliny fuchsinsiřičitej. Po pridaní aldehydu sa kyselina siřičitá uvoľní z fuchsinu a pevnejšie sa naviaže na aldehydovú skupinu. Tento proces vedie k obnoveniu pôvodnej chinoidnej štruktúry a k opätovnému sfarbeniu roztoku do fialova až červena, čo signalizuje prítomnosť aldehydu.
Reakcia s Schiffovým činidlom má významné využitie aj v histológii, napríklad v tzv. PAS reakcii (Periodic Acid - Schiff). Táto metóda sa používa na detekciu glykogénu a iných polysacharidov v tkanivách. Princíp spočíva v oxidácii sacharidov kyselinou jodistou, ktorá následne reaguje s Schiffovým činidlom.
Tvorba Esterov z Alkoholov
Okrem oxidácie a dehydrogenácie sa alkoholy zúčastňujú aj na reakciách esterifikácie. Účinkom minerálnych alebo organických kyselín na alkoholy dochádza k vzniku esterov, ktoré sú anhydridmi oboch zložiek. Pri tejto reakcii sa z molekuly alkoholu a molekuly kyseliny odštiepi molekula vody. Estery sú často charakteristické príjemnou vôňou a nachádzajú sa v prírodných siliciach.
Prehľad a Použitie Najdôležitejších Alkoholov a Aldehydov
Niektoré alkoholy a aldehydy sú vďaka svojim vlastnostiam a reaktivite obzvlášť dôležité v priemysle a v bežnom živote.
Metanol (CH3OH): Je prudko jedovatá kvapalina, ktorá vzniká pri rozkladnej destilácii dreva. Konzumácia metanolu môže spôsobiť oslepnutie a smrť. Priemyselne sa využíva na výrobu formaldehydu, na denaturáciu liehu (aby sa stal nepožívateľným) a ako rozpúšťadlo. Jeho oxidáciou v organizme vzniká toxický formaldehyd a následne kyselina mravčia, ktorá spôsobuje vážne zdravotné problémy.
Etanol (C2H5OH): Je známy aj ako alkohol alebo lieh. Vyrába sa kvasením cukrov alebo škrobov s následnou frakčnou destiláciou, pri ktorej môžu vznikať aj vyššie alkoholy. Alternatívnou cestou výroby je reakcia etylénu. Etanol s vodou tvorí azeotropnú zmes s bodom varu okolo 96 %. Na získanie bezvodého alkoholu je potrebná špeciálna destilácia s prídavkom látok, ktoré viažu vodu (napr. vápno), alebo iné metódy. Etanol je hlavnou zložkou alkoholických nápojov. Používa sa tiež ako rozpúšťadlo, pri výrobe chloroformu, éteru a mnohých ďalších organických zlúčenín. V pečeni sa etanol metabolizuje pomocou enzýmu alkoholdehydrogenázy na acetaldehyd, ktorý je ďalej spracovaný aldehyddehydrogenázami. Etanol sa v malej miere spontánne produkuje aj v ľudskom tráviacom trakte.
Izopropylalkohol (2-propanol): Používa sa predovšetkým na výrobu acetónu.
Cyklanol (cyklohexanol): Vyrába sa synteticky z fenolu a je dôležitou surovinou pre výrobu silónu.
Glycerol (1,2,3-trihydroxypropan): Je sladká, viskózna kvapalina. Má široké uplatnenie vo výrobe kozmetiky, farmácie a tiež pri výrobe výbušnín.
Etylénglykol (1,2-etándiol): Bezfarebná viskózna kvapalina s bodom varu 198 °C. Je jedovatý a jeho požitie spôsobuje nevoľnosť a zvracanie. Používa sa ako nemrznúca zmes a pri výrobe plastov.
Formaldehyd (metanal): Najjednoduchší aldehyd. Používa sa ako dezinfekčný a konzervačný prostriedok, pri výrobe plastov a živíc. S amoniakom môže tvoriť výbušné zmesi.
Acetaldehyd (etanal): Vzniká oxidáciou etanolu. Je dôležitým medziproduktom pri výrobe octu (kyselina octová), farbív a liečiv.
Benzaldehyd: Má charakteristickú mandľovú vôňu. Používa sa pri výrobe farbív, liečiv a kyseliny benzoovej.
Fenoly: Príbuzní Alkoholov s Kyslejšími Vlastnosťami
Fenoly sú organické zlúčeniny, ktoré sa od alkoholov líšia tým, že hydroxylová skupina je priamo viazaná na aromatický (benzénový) kruh. Táto väzba ovplyvňuje ich chemické vlastnosti. Fenoly sú vo všeobecnosti kyslejšie ako alkoholy. Vysvetlenie tejto vyššej kyslosti spočíva v mezomérnom efekte. Po odštiepení protónu z hydroxylovej skupiny fenolu vzniká fenoxidový anión, ktorý je stabilizovaný delokalizáciou záporného náboja na benzénové jadro. Táto stabilizácia uľahčuje odštiepenie protónu, čím sa fenoly správajú ako silnejšie kyseliny.
Príklady dôležitých fenolov a ich derivátov zahŕňajú:
- Fenol: Leptá kožu a používa sa pri výrobe plastov, farieb, liekov a pesticídov.
- Hydrochinón: Používa sa ako fotografická vývojka.
- Kyselina pikrová: Je jedovatá a silne výbušná zlúčenina.
Étery: Odlišné Vlastnosti a Riziká
Étery sú organické zlúčeniny, ktoré majú vo všeobecnosti nízke body varu, sú prchavé a často výbušné. Vyznačujú sa tým, že atóm kyslíka je viazaný na dva uhlíkové atómy, ktoré sú súčasťou organických zvyškov. Étery sú dobrými rozpúšťadlami, ale sú aj pomerne nepolárne a vo vode sa nerozpúšťajú. Zvýšené riziko pri práci s étermi predstavuje ich schopnosť reagovať so vzdušným kyslíkom a slnečným svetlom za vzniku explozívnych peroxidov. Preto sa étery skladujú v tme a v dobre uzavretých nádobách.
Zhrnutie Chemických Vlastností a Reakcií
Alkoholy a aldehydy sú fascinujúce skupiny organických zlúčenín s bohatou chémiou. Primárne alkoholy slúžia ako prekurzory pre aldehydy prostredníctvom dehydrogenácie a môžu byť ďalej oxidované na karboxylové kyseliny. Sekundárne alkoholy sa oxidujú na ketóny. Reakcie ako dehydratácia a esterifikácia rozširujú ich syntetický potenciál. Pochopenie týchto základných transformácií je kľúčové pre rozvoj modernej organickej chémie a jej aplikácií. Rozdiely vo vlastnostiach, ako je kyslosť fenolov oproti alkoholom, alebo reaktivita aldehydov v porovnaní s ketónmi, umožňujú selektívne chemické reakcie a špecifické aplikácie.