Alkény, alkíny a alkadiény predstavujú fascinujúcu triedu organických zlúčenín, ktoré sú základom mnohých chemických procesov a priemyselných aplikácií. Ich charakteristickým znakom je prítomnosť násobných väzieb medzi atómami uhlíka, čo im dodáva jedinečné chemické vlastnosti a reaktivitu. Zatiaľ čo alkány sa vyznačujú výlučne jednoduchými sigma väzbami, nenasýtené uhľovodíky ako alkény (s dvojitou väzbou C=C) a alkíny (s trojitou väzbou C≡C) obsahujú aj pi väzby (π), ktoré sú kľúčové pre ich chemické transformácie. Tieto pi väzby, tvorené prekrytím nehybridizovaných p orbitálov, sú menej stabilné a viac dostupné pre útok reaktívnych činidiel, čo vedie k ich vysokej chemickej reaktivite.
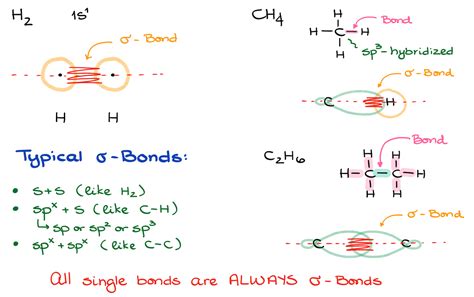
Alkény: Základná stavebná jednotka nenasýtených uhľovodíkov
Alkény sú nenasýtené uhľovodíky, ktoré tvoria homologický rad s všeobecným vzorcom CnH2n. Každý atóm uhlíka v dvojitej väzbe prechádza sp² hybridizáciou, čo vedie k trigonálnej plochej geometrii molekuly s uhlami väzieb približne 120 stupňov. Najjednoduchším zástupcom tejto triedy je etén (C₂H₄), kde sa atómy uhlíka spájajú dvojitou väzbou. Táto štruktúra umožňuje vznik rôznych typov izomérie, ako je cis- a trans-izoméria, ktorá závisí od priestorového usporiadania substituentov okolo dvojitej väzby.
Fyzikálne vlastnosti alkénov sú podobné alkánom - sú nerozpustné vo vode a tvoria kovalentné väzby. Ich chemické vlastnosti sú však výrazne odlišné vďaka prítomnosti dvojitej väzby. Charakteristické reakcie alkénov zahŕňajú elektrofilné a radikálové adície, eliminácie a polymerizáciu.
Elektrofilná adícia: Markovnikovovo pravidlo a jeho implkácie
Jednou z najdôležitejších reakcií alkénov je elektrofilná adícia, pri ktorej dochádza k rozpadu π väzby a vytvoreniu dvoch nových σ väzieb. Tento proces je dvojstupňový. V prvom stupni elektrofilné činidlo (často kladne nabitá častica alebo molekula s polarizovanou väzbou) atakuje π elektróny dvojitej väzby, čím vzniká karbkatiónový medziprodukt. Tento karbkatión je následne napadnutý nukleofilom (elektrónovo bohatou časticou), čo vedie k vytvoreniu konečného produktu.
Pri elektrofilnej adícii na nesymetrické alkény platí Markovnikovovo pravidlo. Toto pravidlo hovorí, že v reakcii halogénvodíka (HX) s nesymetrickým alkénom sa atóm vodíka naviaže na ten atóm uhlíka dvojitej väzby, ktorý má viac vodíkových atómov. Opačný scenár, kde sa činidlo naviaže na miesto s najmenším počtom vodíkov, je známy ako opak Markovnikovho pravidla a môže nastať v špecifických podmienkach, napríklad pri radikálovej adícii HBr.

- Príklad elektrofilnej adície halogénu: Adícia chlóru (Cl₂) na etén v prítomnosti katalyzátora, ako je chlorid hlinitý (AlCl₃), vedie k vytvoreniu dichlóretánu. Katalyzátor pomáha vytvoriť elektrofilný katión chlóru (Cl⁺), ktorý potom reaguje s dvojitou väzbou.
- Príklad elektrofilnej adície halogénvodíka: Adícia chlorovodíka (HCl) na etén vedie k vzniku chlóretánu. V súlade s Markovnikovovým pravidlom (hoci etén je symetrický, princíp platí) sa vodík naviaže na jeden uhlík a chlór na druhý.
- Príklad elektrofilnej adície vody: Adícia vody na alkény v kyslom prostredí (s katalyzátorom ako H₂SO₄) vedie k vzniku alkoholov. Najprv sa naviaže protón (H⁺) z kyseliny na dvojitú väzbu, čím vznikne karbkatión. Ten potom reaguje s molekulou vody, pričom vzniká alkohol po odštiepení protónu.
Radikálová adícia HBr: Odchýlka od Markovnikovovho pravidla
Radikálová adícia bromovodíka (HBr) na alkény je zaujímavým prípadom, kde sa reakcia riadi odlišným mechanizmom ako bežná elektrofilná adícia. V prítomnosti iniciátorov radikálovej reakcie (ako sú peroxidy) sa HBr štiepi na radikály Br• a H•. Radikál brómu (Br•) sa potom pripojí k dvojitej väzbe, čím vznikne stabilnejší uhlíkový radikál. Tento radikál následne reaguje s ďalšou molekulou HBr, pričom sa odštiepi atóm vodíka a regeneruje sa radikál brómu. Výsledkom je produkt, kde sa bróm pripojil na menej substituovaný atóm uhlíka dvojitej väzby, čo je v rozpore s Markovnikovovým pravidlom.

Polymerizácia: Tvorba dlhých reťazcov
Polymerizácia je proces, pri ktorom sa mnohé malé molekuly (monoméry) spájajú do dlhých reťazcov (polymérov). Alkény sú základnými monomermi pre mnohé dôležité polyméry. Napríklad etén polymerizuje za vzniku polyetylénu, široko používaného plastu. Polypropylén vzniká polymerizáciou propénu a polyvinylchlorid (PVC) polymerizáciou vinylchloridu. Tento proces je príkladom viacnásobnej adície.

Alkíny: Trojitá väzba a jej dôsledky
Alkíny sú nenasýtené uhľovodíky s najkratšou trojitou väzbou C≡C. Ich všeobecný vzorec je CnH2n-2. Trojitá väzba je tvorená jednou sigma a dvoma pi väzbami, čo ju robí veľmi pevnou, ale zároveň reaktívnou. Atómy uhlíka v trojitej väzbe majú sp hybridizáciu, čo vedie k lineárnej geometrii molekuly s väzbovým uhlom 180 stupňov.
Fyzikálne a chemické vlastnosti alkínov sú podobné alkénom. Ich reakcie prebiehajú do druhého stupňa, čo znamená, že môžu prijať až dve molekuly činidla. Charakteristické reakcie sú elektrofilné adície.
- Adícia HCl a vody: Podobne ako pri alkénoch, aj pri alkínoch dochádza k elektrofilnej adícii. Adícia HCl na alkín prvotne vedie k vzniku alkénu s jednou dvojitou väzbou. Adícia vody na alkíny, katalyzovaná ortuťnatými soľami v kyslom prostredí, prechádza cez nestabilný vinylalkohol (enol formu), ktorý sa ihneď prešmykuje na stabilnejšiu keto formu, napríklad acetaldehyd z acetylénu. Tieto formy sú príkladom tautomérov.
- Príprava acetylidov: Vodíkové atómy viazané na uhlíkových atómoch v trojitej väzbe majú mierne kyslý charakter a môžu byť nahradené kovmi za vzniku solí nazývaných acetylidy. Niektoré acetylidy, ako acetylid strieborný alebo meďný, sú výbušné. Acetylid vápenatý (karbid vápenatý) sa používa na výrobu acetylénu.
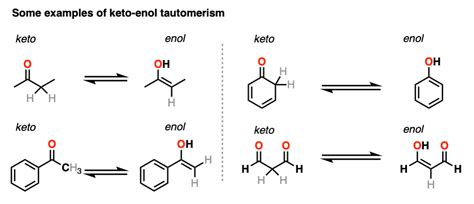
Acetylén: Priemyselný význam a využitie
Acetylén (etín), najjednoduchší alkín, má významné priemyselné využitie. Vyrába sa pyrolýzou metánu a používa sa pri autogénnom zváraní, kde v zmesi s kyslíkom vytvára plameň s extrémne vysokou teplotou. Z acetylénu sa tiež získavajú rôzne organické zlúčeniny. Vzhľadom na jeho nestabilitu pri stlačení sa distribuuje rozpustený v acetóne v poréznej hmote.
Výroba acetylénu (zvárací plyn ⛽️). #chemikálie #chémia #praktické #reakcie
Alkadiény: Dve dvojité väzby v jednej molekule
Alkadiény sú nenasýtené uhľovodíky s dvoma dvojitými väzbami v jednej molekule. Ich chemické vlastnosti sú kombináciou reaktivity alkénov a alkínov, pričom poloha a vzájomné usporiadanie dvojitých väzieb (konjugované, izolované alebo kumulované) ovplyvňujú ich reaktivitu.
Adícia alkohol na alkeny: Špecifický prípad
Hoci v poskytnutých informáciách nie je priamo spomenutá adícia alkoholov na alkeny ako samostatná kapitola, mechanizmus takejto reakcie by sa dal odvodiť z princípov elektrofilnej adície. Alkohol (ROH) by mohol pôsobiť ako elektrofilné činidlo po protonácii (v kyslom prostredí), kde by sa RO⁻ skupina naviazala na karbkatiónový medziprodukt. Alternatívne, ak by sa použil alkohol ako rozpúšťadlo, mohol by reagovať ako nukleofil po aktivácii dvojitej väzby alkénu. Tieto reakcie sú dôležité v organickej syntéze pre tvorbu éterov.

Zhrnutie a širší kontext
Adičné reakcie, či už elektrofilné, radikálové alebo nukleofilné, sú základnými stavebnými kameňmi organickej chémie, ktoré umožňujú premenu jednoduchých molekúl na zložitejšie. Pochopenie mechanizmov týchto reakcií, vrátane pravidiel ako je Markovnikovovo, je kľúčové pre syntézu nových zlúčenín a pre pochopenie chemických procesov v prírode aj v priemysle. Od výroby plastov a liečiv až po syntézu palív a materiálov, adičné reakcie zohrávajú nezastupiteľnú úlohu v modernom svete.