Aldehydy a alkoholy sú dve základné skupiny organických zlúčenín, ktoré zohrávajú kľúčovú úlohu v chémii aj v biológii. Ich vzájomné vzťahy sú komplexné, zahŕňajúce premeny jedného typu na druhý a špecifické reakcie, ktoré sú základom mnohých priemyselných procesov a biologických funkcií. Pochopenie týchto interakcií je nevyhnutné pre aplikovanú chémiu, medicínu a dokonca aj pre pochopenie účinkov bežných látok, ako je etanol.
Klasifikácia a Základné Vlastnosti Alkoholov a Fenolov
Alkoholy patria medzi nearomatické hydroxyderiváty uhľovodíkov, zatiaľ čo fenoly obsahujú hydroxylovú funkčnú skupinu viazanú priamo na benzénový kruh. Hydroxylová skupina (-OH) je kľúčovou funkčnou skupinou, ktorá určuje ich chemické správanie. V závislosti od uhlíka, na ktorý je skupina -OH viazaná, rozlišujeme primárne, sekundárne a terciárne alkoholy.
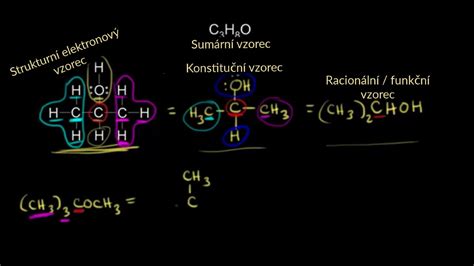
Chemické vlastnosti alkoholov sú do značnej miery ovplyvnené polaritou väzby O-H, ktorá vyplýva z rozdielnej hodnoty elektronegativity kyslíka a vodíka. Táto polarita dodáva alkoholom mierny kyslý charakter. Voči silným kyselinám sa však môžu správať ako zásady, tvoriac alkoxóniové soli. Alkoholy sú teda amfotérne, fungujú ako Bronstedove kyseliny aj zásady.
Fenoly sú v porovnaní s alkoholmi kyslejšie. Toto zvýšené kyslé správanie je vysvetliteľné mezomérnym efektom. Po odštiepení protónu sa výsledný anión stabilizuje delokalizáciou záporného náboja na benzénové jadro, čo uľahčuje jeho vznik.
Reakcie Alkoholov
Alkoholy sa zúčastňujú na širokej škále chemických reakcií, ktoré sú dôležité pre ich syntézu a transformáciu.
Oxidácia Alkoholov
Oxidácia alkoholov je jednou z najdôležitejších reakcií, ktorá umožňuje rozlišovať medzi primárnymi, sekundárnymi a terciárnymi alkoholmi na základe ich oxidačných produktov - aldehydov a ketónov.
- Primárne alkoholy sa pri oxidácii najprv premieňajú na aldehydy. Pri použití silnejších oxidačných činidiel, ako je kyselina chrómová, dichromát draselný alebo manganistan draselný, sa aldehyd ďalej oxiduje na karboxylovú kyselinu. Napríklad, etanol (C2H5OH) sa oxiduje na acetaldehyd (CH3CHO) a následne na kyselinu octovú (CH3COOH).
- Sekundárne alkoholy sa oxidujú na ketóny. Napríklad, propan-2-ol (izopropylalkohol) sa oxiduje na acetón. Ketóny sú voči ďalšej oxidácii odolnejšie ako aldehydy.
- Terciárne alkoholy sú voči oxidácii pomocou bežných oxidačných činidiel v miernych podmienkach viac-menej odolné. V extrémnych podmienkach môžu podliehať štiepeniu C-C väzieb.

Vhodným oxidačným činidlom, ktoré sa často používa na tieto účely, je napríklad chromsírová zmes (zmes koncentrovanej kyseliny sírovej a dichromanu draselného). Reakcia sa vykonáva opatrením zahrievaním zmesi alkoholu a kyseliny chromsírovej.
Dehydratácia Alkoholov
Dehydratácia alkoholov je reakcia, pri ktorej dochádza k odštiepeniu molekuly vody. V závislosti od reakčných podmienok môžu vznikať alkény alebo étery. Reakcia prebieha zahrievaním alkoholu s vhodnými katalyzátormi, ako je koncentrovaná kyselina sírová (H2SO4), pentoxid fosforečný (P2O5) alebo chlorid zinočnatý (ZnCl2). Alternatívne sa môže uskutočniť vedením pár alkoholu cez kontaktný katalyzátor, napríklad oxid hlinitý (Al2O3), pri zvýšenej teplote.
Dehydratácia prebieha najľahšie pri terciárnych alkoholoch a najťažšie pri primárnych. Pri týchto reakciách sa uplatňuje Zajcevovo pravidlo, ktoré predpovedá tvorbu najviac substituovaného alkénu ako hlavného produktu.
Dehydrogenácia Alkoholov
Dehydrogenácia alkoholov nastáva vedením pár alkoholu cez prehriaty kovový katalyzátor, zvyčajne meď alebo striebro. Pri tejto reakcii alkohol stráca dva atómy vodíka. Primárne alkoholy sa premieňajú na aldehydy a sekundárne alkoholy na ketóny. Táto metóda je dôležitá pre syntézu aldehydov a ketónov.
Tvorba Esterov
Estery karboxylových kyselín sa za normálnych okolností vyrábajú z karboxylových kyselín a alkoholov pomocou kyslej katalýzy. Pritom z alkoholu a molekuly kyseliny vystúpi molekula vody. Existuje však aj iný spôsob výroby esterov, a to prostredníctvom Claisenovej-Tiščenkovej reakcie.
Claisenova-Tiščenkova reakcia je chemická reakcia spočívajúca v disproporcionácii aldehydu bez vodíka v alfa-polohe v prítomnosti alkoxidu; produktom reakcie je ester. Reakcia je pomenovaná podľa chemikov L. Claisena a V. Tiščenka. Pri tejto reakcii reaguje aldehyd s hlinitým alkoholátom ako katalyzátorom. Pre neenolizovateľné aldehydy je možné použiť aj alkoxid sodný. Alkoholát sa viaže na dve molekuly aldehydu a vytvorí cyklický prechodný stav, ktorý vedie k vzniku esteru.
Aldehydy a Ich Reakcie
Aldehydy sú organické zlúčeniny obsahujúce funkčnú skupinu -CHO. Táto skupina im dodáva charakteristické vlastnosti a reaktivitu.
Reakcie s Tollensovým, Fehlingovým a Benedictovým Činidlom
Aldehydy redukujú Tollensovo, Fehlingovo alebo Benedictovo činidlo. Tieto reakcie sa využívajú na dôkaz prítomnosti aldehydov.
- Tollensovo činidlo je roztok dvojsubstituovaného komplexu striebra s amoniakom. V prítomnosti aldehydu sa strieborné ióny redukujú na elementárne striebro, ktoré sa vylúči na povrchu nádoby a vytvorí tzv. "zrkadlový povlak".
- Fehlingovo a Benedictovo činidlo sú alkalické roztoky komplexov medi(II) s chelatačnými činidlami (tartarát v prípade Fehlingovho, citrát v prípade Benedictovho). V prítomnosti aldehydu sa modré ióny medi(II) redukujú na červený oxid meďnatý (Cu2O).
Reakcia so Schiffovým Činidlom
Schiffovo činidlo je vodný roztok fialovočerveného farbiva fuchzínu, ku ktorému sa pridáva hydrogensiřičitan alebo siřičitan. Hydrogensiřičitan sa aduje na centrálny uhlíkový atóm farbiva, čím sa naruší chinoidná štruktúra podmieňujúca zafarbenie. Vzniká bezfarebný roztok kyseliny fuchsinsiřičitej. Po pridaní aj malého množstva aldehydu sa z vazby na fuchzín uvoľní kyselina siřičitá, ktorá sa naviaže na aldehydovú skupinu pevnejšou väzbou. Toto opätovné vytvorenie chinoidnej štruktúry vedie k zmenšeniu zafarbenia roztoku. Reakcia sa používa na dôkaz aldehydov.
Reakcia s Schiffovým činidlom sa hojne využíva aj v histológii pri tzv. PAS reakcii (Periodic Acid - Schiff) na prienik glykogénu a ďalších polysacharidov v tkanivách. Princípom je oxidácia sacharidov kyselinou jodistou (HIO4), ktorá štiepi vicinálne dioly (dva hydroxylové skupiny na susedných uhlíkoch) a vznikajú aldehydy, ktoré následne reagujú so Schiffovým činidlom.
Etanol: Vlastnosti, Metabolizmus a Následky Konzumácie
Etanol (etylalkohol, C2H5OH) je najznámejší alkohol, ktorý je súčasťou mnohých alkoholických nápojov, liekov a je tiež produktom kvasenia.
Metabolizmus Etanolu v Organizme
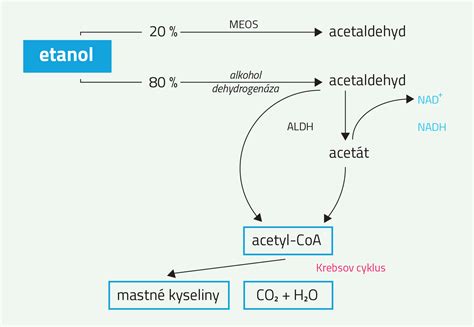
Hlavným systémom pečeňového metabolizmu etanolu je oxidácia v cytoplazme hepatocytov. V prvom kroku sa etanol oxiduje na acetaldehyd enzymom alkoholdehydrogenázou (ADH, EC 1.1.1.1).
C2H5OH + NAD+ → CH3CHO + NADH + H+
Aktivita tohto enzymu je daná geneticky a môže vysvetľovať rôznu individuálnu vnímavosť k alkoholu. Acetaldehyd je veľmi toxická zlúčenina, ktorá je zodpovedná za mnohé nepríjemné účinky konzumácie alkoholu, vrátane príznakov kocoviny. Je karcinogén a môže poškodzovať DNA a proteíny.
Acetaldehyd je následne konvertovaný aldehyddehydrogenázami (ALDH) na menej toxickú kyselinu octovú (acetát).
CH3CHO + NAD+ + H2O → CH3COOH + NADH + H+
Acetaldehyd je 7x toxickejší ako alkohol. Môže reagovať s amino skupinami bielkovín a tvoriť amíny alebo Schiffove bázy. Táto reakcia môže mať za následok inhibíciu enzýmov, napr. aldehyddehydrogenázy a monoaminoxidázy. Inhibícia monoaminoxidázy môže spôsobiť zvýšenie hladiny neuroamínov v krvi po konzumácii etanolu.
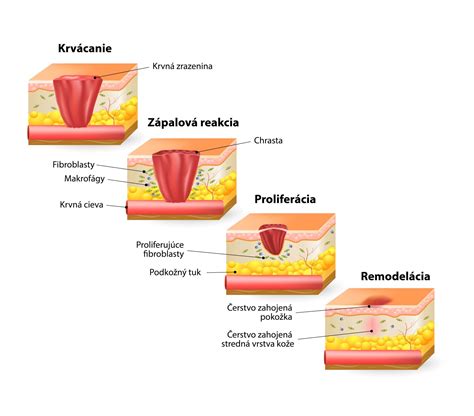
Počas metabolizmu etanolu dochádza k produkcii NADH. Nadbytok NADH reguluje metabolické dráhy a môže viesť k rôznym problémom, napríklad k zníženiu rýchlosti citrátového cyklu a k aktivácii tvorby mastných kyselín v pečeni, čo vedie k hromadeniu tukových kvapôčok a zväčšeniu pečene - ztučneniu pečene. Toto je prvý stupeň poškodenia pečene, ktorý je však vratný. Pri pokračujúcej konzumácii môže dôjsť k alkoholickej hepatitíde a v najhoršom prípade k cirhóze pečene.
Okrem toho, alkohol sám o sebe ovplyvňuje organizmus. Preniká do mozgu a inhibuje vylučovanie antidiuretického hormónu (ADH, vazopresín), ktorý reguluje resorpciu vody v obličkách. Nedostatok ADH vedie k zvýšenému vylučovaniu moču, čo spôsobuje dehydratáciu organizmu, s následnou bolesťou hlavy, únavou a suchom v ústach. Alkohol tiež pôsobí ako sedatívum, utlmuje mozgovú aktivitu a spôsobuje uvoľnenie, stratu zábran, ale aj zníženú schopnosť sústrediť sa a poruchy reči.
Následky Nadmernej Konzumácie Alkoholu
Konzumácia alkoholu patrí podľa WHO medzi najčastejšie rizikové faktory poškodenia zdravia. Dochádza k rozvoju mnohých nežiaducich zdravotných následkov, vrátane alkoholizmu, poškodenia pečene a rôznych druhov rakoviny.
- Poškodenie pečene: Ztučnenie pečene, alkoholická hepatitída, cirhóza.
- Gastrointestinálne problémy: Zvýšená produkcia HCl, histamínu, vznik vredov a rakoviny žalúdka, znížená absorpcia vitamínov v črevách.
- Poškodenie nervového systému: Zvýšené riziko krvácania do mozgu, poškodenie malého mozgu (koordinácia pohybov, rovnováha), kognitívne poruchy.
- Kardiovaskulárne problémy: Zvýšenie krvného tlaku, poškodenie srdcového svalu.
- Rakovina: Alkohol je dokázaný karcinogén. Zvyšuje riziko rakoviny ústnej dutiny, hltana, hrtana, pažeráka, pečene, hrubého čreva a prsníkov. Alkohol a fajčenie majú na riziko rakoviny synergický efekt.
- Teratogénne účinky: Konzumácia alkoholu počas tehotenstva môže viesť k poškodeniu plodu (FAS - Fetálny alkoholový syndróm).
Metanol: Toxický Alkohol
Na rozdiel od etanolu, metanol (metylalkohol, CH3OH) je pre ľudský organizmus vysoko toxický aj v malých dávkach. Po požití 10 ml môže dôjsť k nevratnému poškodeniu zrakového nervu a oslepnutiu, dávka okolo 30 ml je smrteľná.
Príčinou vysokej toxicity metanolu je jeho oxidácia rovnakými enzymatickými systémami ako etanol. ADH premení metanol na formaldehyd (CH2O), ktorý je ešte toxickejší ako metanol. Z formaldehydu vznikne pôsobením ALDH kyselina mravčia (HCOOH). Kyselina mravčia spôsobuje hypoxiu na bunkovej úrovni a metabolickú acidózu, čo vedie k poškodeniu orgánov, najmä zrakového nervu.
CH3OH + NAD+ → CH2O + NADH + H+CH2O + NAD+ + H2O → HCOOH + NADH + H+
Claisenova-Tiščenkova Reakcia a Syntéza Esterov
Claisenova-Tiščenkova reakcia je dôležitým nástrojom pre syntézu esterov. Je to reakcia disproporcionácie aldehydov, ktoré nemajú vodík v alfa-polohe, v prítomnosti silnej zásady, ako je alkoxid. Katalyzátorom býva hlinitý alkoholát alebo alkoxid sodný.
R-CHO + R-CHO → R-COOR' (ester)
Táto reakcia umožňuje priame získanie esterov z aldehydov, čo predstavuje alternatívu k tradičnej esterifikácii karboxylových kyselín alkoholmi.
Azokopulačné Reakcie a Farbivá
Skupina N+≡N je základom pre vznik dusíkového môstku, ktorý spojí v kyslom prostredí arendiazóniovú soľ s fenolickou zlúčeninou. Najjednoduchšou azokopulačnou reakciou je vznik azofarbiva reakciou arendiazóniovej soli s fenolom.
Ar-N2+ + Ar'-OH → Ar-N=N-Ar'-OH + H+
Azoslúčeniny sa vyznačujú bohatým π elektrónovým systémom väzieb. Ak cez tento systém preniká biele svetlo, niektoré vlnové dĺžky sú absorbované a výsledná farba je tvorená neabsorbovanými vlnovými dĺžkami. Relatívne malá zmena v štruktúre azofarbiva môže spôsobiť odlišnú absorpciu vlnových dĺžok a tým aj odlišnú farbu. Táto vlastnosť sa využíva napríklad pri určovaní pH.
Dôležité Alkoholy a Ich Použitie
- Metanol (CH3OH): Rozpúšťadlo, jedovatý, používa sa na priemyselnú výrobu formaldehydu a denaturáciu liehu.
- Etanol (C2H5OH): Alkoholické nápoje, rozpúšťadlo, výroba chloroformu, éteru, liečivá, dezinfekcia.
- Etylénglykol (HOCH2CH2OH): Bezfarebná viskózna kvapalina, nemrznúce zmesi, jedovatý, výroba plastov.
- Glycerol (HOCH2CH(OH)CH2OH): Sladká viskózna kvapalina, výroba kozmetiky, farmácia, výroba výbušnín (nitroglycerín).
- Fenol: Leptá kožu, používa sa na výrobu plastov, farieb, liekov, pesticídov a syntetických vlákien.
- Hydrochinón: Fotografické vývojky.
- Kyselina pikrová: Jedovatá a silne výbušná látka.
Aldehydy v Každodennom Živote a Pri Pôsobení
Aldehydy, ako napríklad acetaldehyd, sú prítomné v mnohých potravinách a nápojoch v dôsledku fermentačných procesov. Sú medziproduktom alkoholového kvasenia, produkovaným kvasinkami. Pre svoju charakteristickú ovocnú vôňu sa často používajú v potravinárstve ako dochucovadlá.
Najvýznamnejším a najväčším rizikom spojeným s aldehydmi je však ich prítomnosť v alkoholických nápojoch a tabaku. Acetaldehyd, ako produkt metabolizmu alkoholu, je hlavnou príčinou symptómov "kocoviny" a je klasifikovaný ako karcinogén skupiny 1.
Výskyt acetaldehydu v životnom prostredí zahŕňa aj výfukové plyny automobilov (kvôli pridávaniu etanolu do palív), nábytok, koberce, textílie a farby. V kuchynských výparoch sa tiež nachádza určité množstvo acetaldehydu.
Preukazovanie Aldehydov
V laboratóriu sa preukazuje prítomnosť aldehydov pomocou Schiffovho činidla. Táto metóda umožňuje kvalitatívne určiť ich prítomnosť vo vzorke. Po pridaní Schiffovho činidla do vzorky, ak sa objaví fialová farba, bola zistená prítomnosť aldehydu.
Aldehydy a Alkoholy v Kontexte Zdravia a Bezpečnosti
Pochopenie reakcií medzi aldehydmi a alkoholmi je kľúčové aj pre zdravotné aspekty. Napríklad, metabolizmus etanolu vedie k tvorbe toxického acetaldehydu, ktorý spôsobuje celú škálu negatívnych účinkov na organizmus. Vedecké štúdie preukázali, že alkohol je karcinogén, a jeho konzumácia by mala byť obmedzená. Odporúčania organizácií ako WHO a rôzne národné zdravotnícke inštitúcie zdôrazňujú potrebu znížiť príjem alkoholu na minimalizáciu rizika zdravotných problémov, vrátane rakoviny.
Metabolizmus alkoholu
V súvislosti s bezpečnosťou pri práci s týmito látkami je nevyhnutné dodržiavať prísne bezpečnostné pravidlá. Nebezpečné vlastnosti, ako je horľavosť acetaldehydu, si vyžadujú špeciálne opatrenia pri skladovaní a manipulácii. Všetky chemické pokusy by mali byť vykonávané len osobami s odborným vzdelaním a pod dohľadom v špecializovaných zariadeniach.