Dva najzákladnejšie a bežne používané alkoholy sú voľným okom nerozoznateľné. Bohužiaľ, táto podobnosť môže viesť k tragickým omylom. Metanol (CH₃OH) a etanol (C₂H₅OH) sú organické zlúčeniny, ktoré hrajú kľúčovú úlohu v mnohých priemyselných odvetviach a v našich životoch. Hoci zdieľajú niektoré základné fyzikálne vlastnosti, ako je bezfarebná kvapalina s charakteristickým štipľavým zápachom a horiacou chuťou, ich chemické vlastnosti a predovšetkým ich vplyv na ľudský organizmus sa dramaticky líšia. Zatiaľ čo etanol je známy svojím využitím v nápojoch a medicíne, metanol predstavuje vážne zdravotné riziko a jeho nesprávne použitie môže mať fatálne následky.
Fyzikálne Vlastnosti a Podobnosti
Alkoholy sú definované ako organické zlúčeniny obsahujúce aspoň jednu hydroxylovú skupinu (-OH) viazanú na nasýtený atóm uhlíka. Moderná chémia ich pozná desiatky, no dve najdôležitejšie z hľadiska humánneho využitia sú metanol a etanol. Obidve sú bezfarebné kvapaliny s charakteristickým štipľavým zápachom a horiacou chuťou. Fyzikálne vlastnosti metanolu a etanolu sa v mnohých aspektoch prekrývajú. Okrem fyzikálneho stavu, farby a vône sa vyznačujú aj mimoriadne dobrou rozpustnosťou vo vode - prakticky neobmedzene. Obidve zlúčeniny majú tiež relatívne nízky bod varu: metanol pri 64,7 °C a etanol pri 78,3 °C. Toto ich robí ľahko odpariteľnými a horľavými.
Metanol aj etanol sú tiež horľavé v akomkoľvek skupenstve. Ich spaľovacie reakcie môžu byť úplné alebo neúplné. Pri úplnom spaľovaní vzniká oxid uhličitý a voda, avšak pri neúplnom spaľovaní, najmä pri nedostatočnom prísune kyslíka, môžu vzniknúť aj jedovaté produkty ako oxid uhoľnatý (CO). Okrem toho nepodliehajú iónovej disociácii vo vode, čo znamená, že vo vodných roztokoch zostávajú vo forme molekúl.
História a Objav
Hoci ľudstvo využíva vlastnosti alkoholov už tisíce rokov, metanol bol objavený až v roku 1661. Dosiahol to britský chemik a fyzik Robert Boyle, ktorý destiloval drevo z Buxusu - odtiaľ alternatívny názov zlúčeniny: drevný lieh. Až v roku 1834 boli francúzski vedci schopní určiť štruktúru molekuly. Vtedy sa zrodil koncept metylalkoholu. Etanol, na druhej strane, je známy už od staroveku vďaka procesu fermentácie, ktorý objavili už starí Egypťania a Rimania.
Metanol: Tichý Zabijak
Z ľudského hľadiska sú dve najdôležitejšie vlastnosti metanolu jeho vysoká toxicita a to, že je výborným rozpúšťadlom. Prvá vlastnosť sa premieta do nebezpečnosti jeho používania, zatiaľ čo druhá určuje jeho široké uplatnenie v priemysle.
Ako jed by sa metanol v žiadnom prípade nemal konzumovať ani vdychovať. Je to preto, že v ľudskom tele sa metabolizuje na vysoko toxické látky, predovšetkým na formaldehyd a následne na kyselinu mravčiu. Už dávka 10 ml sa môže metabolizovať na kyselinu mravčiu, ktorá je extrémne škodlivá. Táto kyselina môže zničiť zrakový nerv a spôsobiť trvalú slepotu. Medzi ďalšie negatívne účinky expozície metanolu patrí hypoxia na bunkovej úrovni (nedostatok kyslíka v tkanivách), metabolická acidóza (nebezpečné okyslenie krvi) a iné poruchy, ktoré môžu dokonca spôsobiť smrť. Za smrteľnú dávku sa považuje už 15 ml čistého metanolu, hoci individuálna citlivosť sa môže líšiť.
Napriek svojej toxicite, pre chemický priemysel je metylalkohol predovšetkým dôležitou zložkou kľúčových reakcií. Vďaka ľahkej premene na formaldehyd, uhľovodíky a metylamín sa používa pri výrobe širokého spektra produktov každodennej potreby. Ročne sa celosvetovo vyrobí až 20 miliónov ton metanolu. Základnou metódou získavania tejto toxickej zlúčeniny však už nie je destilácia dreva, ale hydrogenácia oxidu uhoľnatého (CO) za prítomnosti katalyzátora. Najčastejšie tento proces sprevádza produkciu biomasy.
Metanol sa používa v širokom spektre priemyselných aplikácií:
- Farmaceutický priemysel: Ako surovina pre výrobu liečiv.
- Výroba plastov a syntetických tkanín: Je základnou zložkou pri výrobe mnohých polymérov a vlákien.
- Výroba farbív: Používa sa pri syntéze rôznych farbiacich látok.
- Fungicídy: V poľnohospodárstve ako súčasť prípravkov na ochranu rastlín.
- Fotografické filmy: Kedysi sa používal pri výrobe fotografických materiálov.
- Rozpúšťadlo: Vďaka svojej schopnosti rozpúšťať mnohé organické látky.
- Palivo: V niektorých špecializovaných aplikáciách, často ako zložka palivových zmesí.
Pokiaľ je správne označený a zodpovedne používaný, plní významnú ekonomickú funkciu. Avšak jeho nelegálna výroba a distribúcia, najmä ako náhrada za etanol v alkoholických nápojoch, vedie k častým a tragickým otravám.

Etanol: Univerzálny Pomocník s Rizikami
Z hľadiska chemického zloženia je etanol najbližším príbuzným metanolu. Obsahuje jeden atóm uhlíka a ďalšie dva atómy vodíka v jednej molekule (CH₃CH₂OH). Tento zdanlivo malý rozdiel, teda pridanie jednej metylénovej skupiny (-CH₂-), však čiastočne mení vlastnosti etylalkoholu, vďaka čomu je pre ľudí v určitých kontextoch bezpečnejší. Stojí za to dodať, že toto zabezpečenie môže byť často klamlivé!
Etanol má baktericídne a fungicídne vlastnosti a vo vhodnej koncentrácii (minimálne 70 %) ničí aj vírusy. Podobne ako metanol je účinným rozpúšťadlom a zúčastňuje sa mnohých dôležitých syntéznych reakcií. Zaujímavosťou je, že ho prirodzene produkujú kvasinky v procese metabolizmu cukrov. Tento mechanizmus sa využíva pri kvasení piva a vína.
Najväčšia časť produkcie etanolu sa pripravuje z jednoduchých sacharidov (cukrov) alkoholickým kvasením pôsobením rôznych druhov kvasiniek, predovšetkým rôznych šľachtených kmeňových druhov Saccharomyces cerevisiae. Používa sa k tomu ako cukrový roztok (o maximálnej koncentrácii 20 %), tak aj priamo prírodné suroviny obsahujúce sacharidy, ako sú napr. zemiaky alebo cukrová trstina. Kvalita takto získaného etanolu je veľmi závislá na východiskovej surovine; kvasením vzniká zápara, čiže veľmi zriedený vodný roztok etanolu (maximálne 15 %); vždy však obsahuje nežiaduce prímesi, zrejme vyššie alkoholy (propanol a izopropanol), viac sýtené alkoholy (glycerol), ketóny (acetón) aj. Čistenie sa uskutočňuje na výkonných destilačných kolónach, pričom možno získať tzv. azeotropný alkohol, obsahujúci 95,57 % etanolu a 4,43 % vody. Zvyšok vody môžeme odstrániť destiláciou s bezvodným síranom vápenatým alebo oxidom vápnatým, ktoré vodu viažu alebo dlhodobým pôsobením hygroskopických látok ako napr. bezvodného uhličitanu draselného alebo bezvodného síranu meďnatého (modrej skalice), prípadne molekulových sít. Týmito postupmi možno získať etanol o čistote až 99,9 % (tzv. absolútny alkohol alebo bezvodý etanol, obsahujúci menej nez 0,5 % vody a viac než 99,5 % etanolu).
Inou metódou získavania bezvodého etanolu je priama hydratácia etylénu. Ako katalyzátor sa používa kyselina trihydrogenfosforečná na oxid kremičitom.
Samotný etanol je látka pomerne reaktívna, zvlášť búrlivo reaguje s alkalickými kovmi (sodíkom alebo draslíkom). Produktom tejto reakcie je unikajúci vodík a etoxid sodný (etanolát sodný). Pôsobením oxidačných činidiel (napr. dichromanu draselného v kyslom prostredí) dochádza k oxidácii etanolu na etanal (acetaldehyd) a ďalej na kyselinu etanovú (kyselinu octovú). Premena etanolu na kyselinu octovú prebieha tiež pôsobením mikroorganizmov, hlavne rodu Acetobacter (tzv. octové kvasenie, napr. pri výrobe octu z vína). Priama reakcia s kyslíkom môže prebiehať ako horenie, pri ktorom sa etanol oxiduje až na oxid uhličitý a vodu. Pôsobením halogénvodíkov na etanol dochádza k náhrade hydroxylovej skupiny príslušným halogénovým atómom; napr. účinkom bromovodíku vzniká bromoetán (etylbromid). Podobne vzniká dietyléter aj pôsobením iných silných anorganických kyselín, napr. kyseliny sírovej. Pôsobením halogenidov karboxylových kyselín na etanol vznikajú estery etanolu a príslušnej organickej kyseliny. Napr. reakciou s chloridom acetylu vzniká etylacetát.
Okrem výroby alkoholických nápojov je jednou z najdôležitejších oblastí použitia etanolu medicína. Primárne sa používa na dezinfekciu a rozpúšťanie vo vode nerozpustných liečivých látok. Niekedy sa používa aj ako protijed pri otrave metanolom, kde jeho prítomnosť v tele spomaľuje metabolizmus metanolu na toxické produkty.
Etanol sa používa aj pri výrobe:
- Automobilového a raketového paliva: Ako biopalivo, ktoré zlepšuje výkon a znižuje emisie. Má antidetonačné vlastnosti.
- Palivových článkov: Ako zdroj energie.
- Rozpúšťadiel: V rôznych priemyselných procesoch a pri výrobe farieb, značkovačov a produktov osobnej starostlivosti.
- Výťažkov: Umožňuje efektívnu extrakciu olejov z prírodných surovín, napr. konope.
- Laboratórnych činidiel: V laboratóriách sa používa na zníženie teploty používaných látok v chladiacich zmesiach.
V oblasti kozmetiky sa uplatňuje pri výrobe voňaviek. Tento alkohol má svoje miesto aj pri výrobe čistiacich prostriedkov, napr. prostriedkov na čistenie skla.
How Ethanol is Made
Bezpečnostné Aspekty a Riziká
Bohužiaľ, hoci nie je toxický ako metanol, etylalkohol v skutočnosti spôsobuje každým rokom viac úmrtí. Konzumovaný vo forme nápojov ako pivo, víno a vodka je príčinou až 20 % tragických dopravných nehôd. Okrem toho súvisí s ďalšími vážnymi zraneniami, samovraždami a ťažkými chorobami. Sú to psychoaktívne vlastnosti etanolu, ktoré sú primárne zodpovedné za negatívne účinky konzumácie alkoholu. Ako látka inhibujúca centrálny nervový systém na jednej strane poskytuje pocit relaxácie a na druhej strane spôsobuje poruchy rovnováhy, spomalenie reflexov a dehydratáciu. Znižuje tiež koncentráciu, oslabuje pamäť a vo veľkom množstve vedie k otravám. Z dlhodobého hľadiska je etanol návykový a vedie k rozvoju depresie, sociálnych patológií a kriminality. Na zoznam karcinogénnych látok pre ľudí ho zaradila aj Svetová zdravotnícka organizácia. Pitie alkoholu zvyšuje riziko vzniku rakoviny pažeráka, žalúdka, hrubého čreva, pankreasu a pečene.
Etanol určený pre iné použitie ako na priamu konzumáciu, príp. na výrobu alkoholických nápojov, sa denaturuje (doslova sa pozbavuje prirodzených vlastností). Dôvody sú ekonomicko-právne: na konzumný etanol je na Slovensku (podobne, ako v mnohých iných štátoch) uvalená vysoká spotrebná daň, preto sa do etanolu predávaného na technické účely pridávajú pre človeka toxické látky, aby sa tak mohla obísť spotrebná daň. Etanol sa väčšinou denaturuje metanolom, benzínom, benzénom, izopropanolom, acetónom a inými látkami v závislosti na cieľovom použití. Spotrebná daň z liehu je v súčasnosti na úrovni 1 080 eur v základnej a 540 eur v zníženej sadzbe na hektoliter prepočítaného 100 % etanolu. Povinnosti súvisiace s denaturovaním liehu upravuje v súčasnosti zákon č. 530/2011 Z.z. o spotrebnej dani z alkoholických nápojov v znení neskorších predpisov. Na Slovensku povolené denaturačné prostriedky určené na osobitnú denaturáciu liehu a zmesi denaturačných prostriedkov určených na úplnú denaturáciu liehu upravuje vyhláška Ministerstva financií SR č. 538/2011 Z. z.
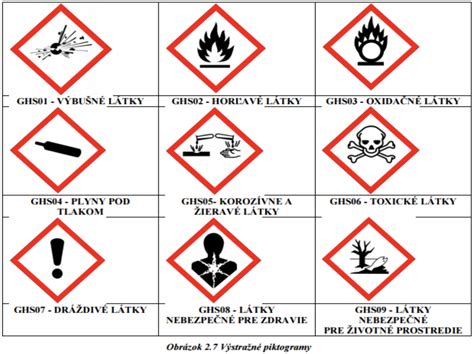
Ak sa na vašom pracovisku zachádza s hořlavými látkami, je zcela nezbytné, aby všetci zamestnanci, ktorí s nimi prídu do styku, poznali a chápali všetky bezpečnostné riziká s tým súvisiace. Jednou z najdôležitejších vecí je poznať rozdiel medzi horľavou a vysoko horľavou látkou. Úroveň rizika, ktorú daná látka predstavuje a fakt, ako ľahko môže spôsobiť požiar, je často ovplyvnený tým, či je látka horľavá alebo vysoko horľavá. Horľavé a vysoko horľavé látky sa nachádzajú takmer na každom pracovisku. Ide najmä o pohonné hmoty, ako je nafta alebo benzín, ale tiež rôzne lepidlá, riedidlá, rozpúšťadlá, čistiace prostriedky, farby, laky, vosky a leštidlá. Každý, kto s týmito a inými nebezpečnými látkami manipuluje, musí byť preškolený z hľadiska bezpečnosti práce (BOZP) a požiarnej ochrany (PO).
Horľavé a vysoko horľavé látky sa líšia v závislosti na teplotách, ktorým musia byť vystavené, aby sa mohli vznietiť, teda horieť. Pamätajte si, že vysoko horľavé látky sa vznietia pri nižších teplotách než horľavé látky. Bod vzplanutia je najnižšia teplota, pri ktorej nebezpečné látky vytvárajú pary a vznietia sa. Teplota vzplanutia je najnižšia teplota, pri ktorej sa vytvorí nad hladinou horľavej kvapaliny pary, ktoré keď sa zmiešajú so vzduchom a priblížia sa k plameňu, vzplanú a hneď sa uhasia. Teplota vznietenia je najnižšia teplota, pri ktorej sa zmes pár alebo plynov danej látky so vzduchom vznieti, teda začne horieť. Teplota vznietenia je zároveň kritériom pre kategorizáciu látok do teplotných tried podľa ČSN 33 0371. Súčasné bezpečnostné listy by mali obsahovať ucelené informácie o danej látke, napr. bodu vzplanutia telivých kvapalín, ktoré sú klasifikované ako horľavé. Zamestnávatelia a zamestnanci by ich mali používať ako zdroj informácií o nebezpečnosti a bezpečnostných opatreniach.
Substitúcia je jedným z prvých krokov v hierarchii kontroly. Nech už skladujete nebezpečné látky kdekoľvek, je pre odstránenie ich pár z budovy rozhodujúca ventilácia - dostatočné odvetrávanie. Zaistite, aby nebezpečné látky boli skladované na mieste s dostatočnou požiarnou odolnosťou a aby nikdy nepresahovali maximálnu povolenú kapacitu skladu. Je veľmi dôležité skladovať horľavé látky a vysoko horľavé látky v uzavretých nádobách, ako je sklo alebo plast. Ak to nie je možné, musia byť kontajnery náležite uzemnené, aby sa zabránilo statickému náboju. Ak môžete kontrolovať teplotu skladu pomocou termostatu, aby ste obmedzili výpary, pozorne ju sledujte.
Teplota Vzplanutia a Varenie s Alkoholom
Ak veríte starej kulinárskej múdrosti, že hovädziemu perkeltu neuškodí trocha červeného vína, alebo malé množstvo tvrdého omáčke k cestovinám, pretože sa aj tak odparí, nemáte celkom pravdu. Pozrime sa na celú problematiku z odborného hľadiska. Teplota varu etanolu je 78,37 °C. Pri varení všeobecne používame oveľa vyššie teploty, napríklad preto, aby nám zovrela voda, čo sa deje pri 100 stupňoch.
Americké ministerstvo poľnohospodárstva (USDA) v roku 1992 iniciovalo sériu niekoľkých výskumov, s cieľom zistiť, aké množstvo alkoholu zostáva v jedlách po ukončení varenia. Zistili, že to závisí od viacerých faktorov, ale z pridaného alkoholu počas varenia, zostáva v jedlách 5-85 percent. Pravidelné miešanie jedla urýchľuje odparovanie alkoholu, takže po 15-minútovom varení v ňom zostáva 40 percent, po polhodine 35, po hodine 25, po dvoch hodinách 10 a po dva a pol hodinách varenia 5 percent alkoholu. Vysvetlením by mohlo byť, že časť alkoholu vytvára s vodou v jedle takzvanú azeotropickú zmes. Čiže v pokrmoch s alkoholom zostáva určité množstvo aj po uvarení. Napriek tomu nie je jednoduché opiť sa napríklad z hovädzieho perkeltu s červeným vínom. Ak skonzumujeme väčšie množstvo alkoholu, zvyšný alkohol sa dostáva do krvného obehu, kde počká, kým ho pečeň neodbúra. Lenže z krvného obehu sa dostáva aj do mozgu, kde manipuluje s komunikáciou medzi mozgovými bunkami - tento jav poznáme ako opilstvo.
Gélové Palivo: Etanol a Metanol v Aplikácii
Želé palivo, tiež známe ako gélové palivo, si získalo významnú obľubu v rôznych aplikáciách, od kempingových varičov až po odieranie riadu v pohostinstve. Typ použitého kvapalného paliva je primárnym faktorom. Želé palivá na báze etanolu majú vo všeobecnosti odlišné charakteristiky topenia v porovnaní s palivami na báze metanolu. Etanol má nižšiu teplotu varu (78,37 °C) ako metanol (64,7 °C), čo môže ovplyvniť teplotu topenia gélu. Okrem toho zohráva dôležitú úlohu koncentrácia alkoholu v géli a typ použitého gélovacieho činidla. Niektoré želé palivá môžu obsahovať prísady na rôzne účely, ako je zvýšenie rýchlosti horenia, zlepšenie zápachu alebo zvýšenie stability gélu. Tieto prísady môžu ovplyvniť teplotu topenia. Napríklad, ak má aditívum vysoký bod topenia, môže zvýšiť celkový bod topenia želé paliva.
Hoci vplyv vonkajšieho tlaku na teplotu topenia želé paliva je relatívne malý v porovnaní s inými faktormi, stále existuje. Podľa princípov termodynamiky zvýšenie tlaku vo všeobecnosti zvyšuje teplotu topenia látok. Vo všeobecnosti sa teplota topenia bežných želé palív na báze etanolu používaných na odieranie riadu a malých vykurovacích zariadení pohybuje približne od 40 °C do 60 °C. Želé palivá na báze metanolu môžu mať mierne nižšie teploty topenia, zvyčajne v rozmedzí 30 °C až 50 °C.
Znalosť teploty topenia želé paliva je nevyhnutná pre správne skladovanie. Ak teplota skladovania prekročí bod topenia, želé palivo sa môže zmeniť na kvapalný stav, čo môže viesť k úniku a potenciálnemu ohrozeniu bezpečnosti. Napríklad, ak sa nádoba s želé palivom roztopí a vytečie v skladovacom priestore, môže vzniknúť riziko požiaru. Pochopenie bodu topenia počas používania pomáha zaistiť optimálny výkon. Napríklad pri aplikácii trecieho taniera, ak je zdroj tepla príliš intenzívny a spôsobuje príliš rýchle topenie želé paliva, môže to mať za následok nerovnomerné horenie a kratší čas horenia.
Niektorí výrobcovia ponúkajú rôzne typy gélového paliva, vrátane:
- Nádrž na tuhý alkohol: Navrhnutá s ohľadom na bezpečnosť a pohodlie.
- Etanolové tuhé gélové palivo na odieranie: Environmentálne šetrná možnosť, vyrobená z vysoko čistého etanolu a netoxického gélovacieho činidla, ktoré zaisťujú čisté a efektívne horenie.
- Opätovne použiteľné konzervované 2h/3h gél alkohol pasta/metanolové palivo: Bezdimové, bez zápachu a netoxické palivo určené na dlhodobé používanie a poskytujúce stály tepelný výkon.

Zhrnutie
Metanol a etanol, hoci sú chemicky podobné, predstavujú dva odlišné svety z hľadiska ich vplyvu na človeka a ich aplikácií. Metanol je vysoko toxický a jeho nesprávne použitie môže viesť k vážnemu poškodeniu zdravia a smrti. Etanol, hoci je vnímaný ako menej nebezpečný, má svoje vlastné vážne zdravotné a sociálne dôsledky pri nadmernej konzumácii. Obidva alkoholy sú však nenahraditeľnými surovinami v mnohých priemyselných odvetviach, pričom ich správne označenie, skladovanie a zodpovedné používanie sú kľúčové pre minimalizáciu rizík a maximalizáciu ich prínosov pre spoločnosť.