Alkoholy predstavujú rozsiahlu a mimoriadne dôležitú triedu organických zlúčenín, ktoré nachádzajú uplatnenie v nespočetných oblastiach ľudskej činnosti - od bežných spotrebných výrobkov až po zložité priemyselné procesy. Ich chemická podstata, definovaná prítomnosťou hydroxylovej skupiny (-OH) viazanej na uhľovodíkový zvyšok, im prepožičiava jedinečné fyzikálne a chemické vlastnosti, ktoré ich robia nenahraditeľnými v mnohých aplikáciách. Hoci pojem "alkohol" často evokuje predstavu alkoholických nápojov, jeho chemický význam je oveľa širší a zahŕňa široké spektrum zlúčenín s rozličnými vlastnosťami a využitím.
Chemická štruktúra a klasifikácia alkoholov
Alkoholy sú deriváty uhľovodíkov, v ktorých je jeden alebo viac atómov vodíka nahradených hydroxylovou skupinou (-OH). Ich všeobecný vzorec je R-OH, kde R reprezentuje alkylovú alebo inú organickú skupinu a -OH je charakteristická hydroxylová funkčná skupina. Je dôležité rozlišovať alkoholy od fenolov, kde je hydroxylová skupina priamo viazaná na aromatický kruh, čo im dodáva odlišné chemické vlastnosti napriek prítomnosti rovnakej funkčnej skupiny.
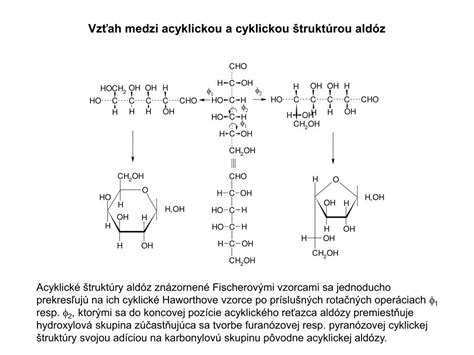
Alkoholy tvoria takzvaný homologický rad, čo znamená, že ich štruktúra sa postupne mení pridávaním opakujúcich sa jednotiek, zvyčajne metylénovej skupiny (-CH2-). Prvé dva členy tohto radu, metanol (CH3OH) a etanol (C2H5OH), sú najznámejšie a najčastejšie používané.
Klasifikácia alkoholov je založená na dvoch hlavných kritériách:
Počet hydroxylových skupín:
- Monohydroxidové alkoholy (jednosýtené): Obsahujú jednu hydroxylovú skupinu (napr. metanol, etanol).
- Polyhydroxidové alkoholy (viacsýtené): Obsahujú dve alebo viac hydroxylových skupín. V závislosti od počtu -OH skupín sa ďalej delia na dioly (dve -OH skupiny, napr. etylénglykol), trioly (tri -OH skupiny, napr. glycerol) a podobne.
Typ uhlíkového atómu, na ktorý je viazaná hydroxylová skupina:
- Primárne alkoholy: Atóm uhlíka viazaný na -OH skupinu je zároveň viazaný na jeden ďalší atóm uhlíka (napr. etanol). Tieto alkoholy sú vďaka svojej reaktivite nevyhnutné v mnohých chemických reakciách a môžu byť oxidované na aldehydy a ďalej na karboxylové kyseliny.
- Sekundárne alkoholy: Atóm uhlíka viazaný na -OH skupinu je zároveň viazaný na dva ďalšie atómy uhlíka (napr. izopropanol). Oxidáciou sekundárnych alkoholov vznikajú ketóny.
- Terciárne alkoholy: Atóm uhlíka viazaný na -OH skupinu je zároveň viazaný na tri ďalšie atómy uhlíka. Terciárne alkoholy sú v porovnaní s primárnymi a sekundárnymi alkoholmi menej reaktívne.
Je dôležité poznamenať, že dve alebo viac hydroxylových skupín na jednom uhlíkovom atóme sú zvyčajne nestabilné a označujú sa ako geminálne dioly.
Výroba a získavanie alkoholov
Metódy získavania alkoholov sú rozmanité a často technicky náročné, vyžadujúce špecifické podmienky a často aj špecializované katalyzátory. V priemyselnom meradle sa najčastejšie vyrábajú metanol, etanol, etylénglykol a glycerol.
- Metanol (drevený lieh): Historicky sa vyrábal destiláciou dreva. V súčasnosti sa jeho produkcia uskutočňuje synteticky katalytickou hydrogenáciou oxidu uhoľnatého pri zvýšenom tlaku a teplote (300-400 °C). Syntetický metanol je významnou surovinou pre chemický priemysel.
- Etanol (etylalkohol): Najčastejšie sa vyrába alkoholovým kvasením surovín bohatých na cukry alebo škroby (napr. obilie, zemiaky, cukrová trstina). Rastlinné suroviny obsahujúce škrob sa najprv štiepia na jednoduchšie cukry, ktoré následne kvasia pôsobením kvasiniek (predovšetkým Saccharomyces cerevisiae). Výsledná zmes, tzv. zápara, s maximálnym obsahom etanolu do 15 %, sa ďalej spracováva destiláciou, čím sa získava destilát s obsahom etanolu 80-90 %. Pre získanie vysoko čistého etanolu, vrátane absolútneho (bezvodého) alkoholu, sa používajú pokročilé destilačné techniky a metódy na odstraňovanie vody, ako je použitie bezvodých solí alebo molekulových sít. Alternatívnou metódou získavania bezvodého etanolu je priama hydratácia etylénu, kde sa ako katalyzátor používa kyselina trihydrogenfosforečná na oxid kremičitom.
- Polyhydroxidové alkoholy:
- Etylénglykol a propylénglykol: Vyrábajú sa procesom hydrolýzy epoxidov.
- Glycerol: Je vedľajším produktom hydrolýzy tukov, ako aj pri výrobe polypropylénu alebo akroleínu.
Fyzikálne a chemické vlastnosti alkoholov
Polarita hydroxylovej skupiny (-OH) je kľúčová pre pochopenie fyzikálnych vlastností alkoholov. Vďaka rozdielu v elektronegativite medzi atómami kyslíka a vodíka v tejto skupine sú molekuly alkoholov polárne. Táto polarita umožňuje tvorbu vodíkových väzieb medzi molekulami alkoholov v kvapalnom stave, podobne ako vo vode. Vodíkové väzby spôsobujú asociáciu molekúl, čo vedie k vyšším teplotám varu v porovnaní s inými organickými zlúčeninami podobnej molekulovej hmotnosti. Napríklad etanol má bod varu 78,37 °C.
- Rozpustnosť: Metanol, etanol a propanol sú miešateľné s vodou v akomkoľvek pomere vďaka schopnosti tvoriť vodíkové väzby s molekulami vody. Rozpustnosť butanolu, ktorý má dlhší uhľovodíkový reťazec, je však už výrazne nižšia (cca 8 g/dm³). S predlžujúcim sa uhľovodíkovým reťazcom klesá rozpustnosť alkoholov vo vode.
- Fyzický stav a zápach: Väčšina nižších alkoholov sú kvapaliny s charakteristickým zápachom. Alkoholy s dlhými uhľovodíkovými reťazcami sa však v závislosti od dĺžky reťazca môžu vyskytovať aj v pevnom skupenstve.
- Chemické vlastnosti: Alkoholy podliehajú širokej škále chemických premen.
- Reakcia s kovmi: V bezvodom prostredí reagujú alkoholy s alkalickými kovmi (napr. sodíkom) za vzniku alkoholátov (alkoxidov), čo sú silné zásady. Napríklad reakcia etanolu so sodíkom vedie k vzniku etoxidu sodného a uvoľneniu vodíka.
- Kyslosť/zásaditosť: Z chemického hľadiska sú alkoholy považované za veľmi slabé kyseliny (slabšie ako voda). Ich zásadité vlastnosti súvisia s voľnými elektrónovými pármi na atóme kyslíka v hydroxylovej skupine.
- Oxidácia: Primárne alkoholy môžu byť oxidované na aldehydy a ďalej na karboxylové kyseliny. Sekundárne alkoholy sa oxidáciou premieňajú na ketóny.
- Dehydratácia: V prítomnosti kyselín môžu alkoholy dehydratovať za vzniku alkénov.
- Esterifikácia: Reagujú s karboxylovými kyselinami za vzniku esterov.
- Halogenácia: Reakciou s halogenovodíkmi dochádza k substitúcii hydroxylovej skupiny halogénovým atómom.
- Horenie: Pri spaľovaní sa alkohol, ako napríklad etanol, premieňa na oxid uhličitý a vodu.
Využitie alkoholov
Všestrannosť alkoholov sa prejavuje v ich širokom uplatnení v rôznych priemyselných odvetviach a v každodennom živote.
Fermentácia etanolu | Proces tvorby alkoholu
- Rozpúšťadlá: Alkoholy, najmä etanol, sú vynikajúce rozpúšťadlá pre polárne aj nepolárne látky, ktoré nie sú rozpustné vo vode. Používajú sa v laboratórnych aj priemyselných aplikáciách, vrátane výroby farieb, lakov, lepidiel a farmaceutických prípravkov.
- Palivá: Etanol je významným biopalivom, ktoré sa používa samostatne alebo v zmesiach s benzínom. Jeho použitie ako paliva je podporované snahou o zníženie závislosti na fosílnych palivách a znižovanie emisií. Hoci náklady na výrobu energie z biopalív môžu byť v súčasnosti vyššie, očakáva sa ich rastúca ekonomická atraktivita. Využitie liehových destilátov ako paliva je obzvlášť vhodné v oblastiach s obmedzeniami používania tuhých palív.
- Suroviny a medziprodukty v chemickom priemysle: Metanol je kľúčovou surovinou pre syntézu formaldehydu, kyseliny octovej a metylesterov. Etanol slúži na výrobu kyseliny etánovej a etylesterov.
- Potravinársky priemysel: Etanol je súčasťou alkoholických nápojov a používa sa aj ako konzervačná látka.
- Kozmetika a parfuméria: Etanol je bežnou zložkou parfumov, dezodorantov, make-upov a iných kozmetických výrobkov, kde pôsobí ako rozpúšťadlo a antibakteriálne činidlo.
- Farmaceutický priemysel: Etanol sa používa ako rozpúšťadlo pre niektoré liečivá (napr. jódová tinktúra) a pri príprave rôznych liečivých prípravkov. Používa sa aj na dezinfekciu neporanenej kože.
- Čistiace a dezinfekčné prostriedky: Denaturovaný lieh je základnou zložkou mnohých čistiacich a dezinfekčných prostriedkov.
- Výroba plastov a iných materiálov: Alkoholy hrajú rolu pri výrobe esterov, ktoré sa používajú pri výrobe plastov.
- Potravinársky priemysel: Etanol je prísadou do niektorých druhov alkoholických nápojov a tiež ako konzervačná látka.
- Biologické systémy: Hydroxylové skupiny sú kľúčové pre funkciu mnohých biologických molekúl, napríklad sacharidov, ktoré sú nevyhnutné pre skladovanie a prenos energie v živých organizmoch.
Bezpečnosť a manipulácia s alkoholmi
Napriek ich užitočnosti a všestrannosti sú alkoholy nebezpečné zlúčeniny, ktoré si vyžadujú zodpovedné a bezpečné zaobchádzanie.
- Toxicita: Nie všetky alkoholy sú bezpečné na konzumáciu. Etanol je v malom množstve bezpečný pre ľudskú spotrebu, ale jeho nadmerná konzumácia má škodlivé účinky na centrálny nervový systém. Metanol je vysoko toxický a jeho požitie môže viesť k vážnym zdravotným problémom, vrátane slepoty a smrti. Preto je nevyhnutné rozlišovať medzi rôznymi typmi alkoholov a poznať ich špecifické vlastnosti.
- Skladovanie a preprava: Alkoholy musia byť počas celého procesu od výroby po dodanie spotrebiteľovi správne skladované a prepravované, aby sa zabránilo kontaminácii alebo úniku. Faktory ako správna teplota a blízkosť iných chemikálií sú kľúčové pre bezpečnosť.
- Denaturácia: Etanol určený na technické účely (nie na konzumáciu) sa denaturuje (chemicky upravuje) pridaním toxických látok, ako je metanol, benzín alebo acetón. Dôvodom je obchádzanie vysokej spotrebnej dane, ktorá je uvalená na konzumný etanol.
- Nakladanie s odpadom: Odpad vznikajúci pri výrobe, spracovaní alebo používaní alkoholov podlieha špeciálnym pravidlám likvidácie. Odporúča sa kontaktovať špecializované firmy na bezpečnú likvidáciu chemického odpadu.
Pochopenie chemických vlastností a potenciálnych rizík spojených s alkoholmi je nevyhnutné pre ich bezpečné a efektívne využitie vo všetkých oblastiach, kde nachádzajú svoje uplatnenie.