Izopropylalkohol, známy aj ako propan-2-ol alebo IPA, je bežná organická zlúčenina s chemickým vzorcom C₃H₈O. Je to bezfarebná, horľavá kvapalina charakteristického zápachu, ktorá patrí do skupiny sekundárnych alkoholov. Vďaka svojim jedinečným chemickým vlastnostiam a širokej dostupnosti nachádza uplatnenie v mnohých priemyselných odvetviach. Jedným z kľúčových procesov, pri ktorých sa izopropanol využíva, je spaľovanie, ktoré vedie k produkcii plynov a uvoľňovaniu tepla.
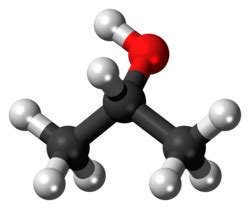
Chemické Vlastnosti a Výroba Izopropanolu
Izopropylalkohol je najjednoduchším príkladom sekundárneho alkoholu, kde je karbónový atóm nesúci hydroxylovú skupinu viazaný na dva ďalšie karbónové atómy. Je izomérom 1-propanolu. Vyrába sa z propénu a vody prostredníctvom dvoch hlavných procesov: nepriamej hydratácie pomocou kyseliny sírovej alebo priamej hydratácie za prítomnosti katalyzátorov. Nepriamy proces, ktorý umožňuje použitie menej kvalitného propénu, dominuje v Spojených štátoch, zatiaľ čo priamy proces, vyžadujúci vysoko čistý propén, je bežnejší v Európe. Oba procesy si vyžadujú následnú destiláciu na izoláciu izopropanolu z vody a vedľajších produktov.
Izopropanol je miešateľný s vodou, etanolom a chloroformom, pretože je to polárna organická molekula. Rozpúšťa širokú škálu nepolárnych zlúčenín, vrátane etylcelulózy, polyvinylbutyralu, mnohých olejov, alkaloidov a prírodných živíc. Na rozdiel od metanolu alebo etanolu nie je miešateľný s roztokmi solí, čo umožňuje jeho separáciu z vodných roztokov pridaním soli, ako je chlorid sodný. Izopropanol tvorí s vodou azeotropickú zmes s teplotou varu 80,37 °C, obsahujúcu 87,7 % hmotnostných (91 % v/v) izopropanolu.
Spaľovanie Izopropanolu: Produkcia CO₂ a Tepla
Spaľovanie izopropanolu je exotermická reakcia, pri ktorej reaguje s kyslíkom za vzniku oxidu uhličitého (CO₂) a vody (H₂O), pričom sa uvoľňuje značné množstvo tepla. Rovnica tejto reakcie je:
2C₃H₈O + 9O₂ → 6CO₂ + 8H₂O
Táto reakcia produkuje oxid uhličitý, ktorý môže byť užitočný vo vysokoteplotných a vysokoenergetických priemyselných prostrediach. Izopropanol tak môže v týchto kontextoch slúžiť ako palivo alebo zdroj plynu. Oxid uhličitý generovaný pri spaľovaní izopropanolu je podobný tomu, ako pri etanole, ale etanol zvyčajne uvoľňuje viac tepla.

Okrem spaľovania môže izopropanol pri vysokých teplotách podliehať aj tepelnému rozkladu (pyrolýze), čím sa vytvárajú menšie molekuly, ako je propylén (etylén) a metán. Táto reakcia rozkladu, známa aj ako krakovanie pri vysokej teplote, nie je primárnym spôsobom výroby plynu v priemyselných aplikáciách, ale je dôležitá pre pochopenie celkovej reaktivity zlúčeniny.
Priemyselné Využitie Izopropanolu v Súvislosti so Spaľovaním
V priemyselných scenároch, ktoré vyžadujú plyny (ako je oxid uhličitý) a teplo, môže izopropanol pôsobiť ako chemické palivo. Menej bežne sa však používa na výrobu čistého plynu a primárne sa využíva na oxid uhličitý vznikajúci pri spaľovaní. Jeho aplikácie sú široké:
- Rozpúšťadlo a čistiaci prostriedok: Izopropanol je vynikajúcim rozpúšťadlom pre širokú škálu nepolárnych zlúčenín. Je relatívne netoxický a rýchlo sa odparuje, čo ho robí ideálnym pre čistenie elektronických zariadení, ako sú elektrické kontakty, magnetické hlavy, laserové šošovky optických mechaník, a na odstraňovanie teplovodivých pást z CPU. Používa sa aj na čistenie LCD a sklenených obrazoviek, hoci s určitým rizikom pre antireflexné vrstvy. Hudobné obchody ho používajú na leštenie gramofónových platní a na odstraňovanie nežiaducich atramentových značiek z povrchov. Je účinný pri odstraňovaní zvyškov lepidla po nálepkách a pri čistení zbraní. Dobre odstraňuje šmuhy, špinu a odtlačky prstov z mobilných telefónov a PDA.
- Konzervant: V porovnaní s čistým etanolom poskytuje izopropanol lacnejšiu a porovnateľne netoxickú alternatívu k formaldehydu a iným syntetickým konzervantom pre biologické preparáty. Dezinfekčné vankúšiky typicky obsahujú 60-70 % roztok izopropanolu vo vode.
- Prísada do benzínu: Izopropanol je hlavnou zložkou aditív pre odvodňovanie benzínu. Pomáha rozpúšťať vodu v benzíne, čím zabraňuje jej zamrznutiu v palivovom systéme.
- Ofsetová tlač: V ofsetovej tlači sa používa ako prísada na zníženie povrchového napätia vlhčiaceho roztoku, v moderných systémoch až do 5 %.
- Chemická syntéza: Ako sekundárny alkohol môže byť oxidovaný na ketón, acetón. Reaguje s aktívnymi kovmi, ako je draslík, za vzniku alkoxidov, nazývaných izopropoxidy.
- Palivo pre bufety a ohrievače: Izopropylalkohol, vzhľadom na svoju horľavosť a relatívne nízky bod vzplanutia (okolo 11-12 °C), sa používa v niektorých palivách pre bufetové ohrievače a prenosné variče. V týchto aplikáciách sa často používa vo forme gélu alebo pasty, ktorá je menej náchylná na rozliatie. Spaľovanie prebieha ako chemická reakcia s kyslíkom, uvoľňujúca teplo a svetlo vo forme plameňa.
Čo neznášajú ploštice a ako vyzerajú štípance od ploštíc
Porovnanie s Etanolom a Peroxidom Vodíka
Je dôležité rozlišovať izopropanol od iných bežných chemikálií s podobným použitím, ako sú etanol a peroxid vodíka.
- Etanol (C₂H₅OH): Etanol sa spaľuje podobne ako izopropanol, produkujúc oxid uhličitý a vodu, ale zvyčajne uvoľňuje viac tepla, čo z neho robí vhodnejšie palivo pre scenáre s rozsiahlym spaľovaním. Okrem spaľovania sa etanol využíva aj v parnej reformácii na výrobu vodíka (H₂) a oxidu uhoľnatého (CO) pomocou reakcie: C₂H₅OH + H₂O → CO + 3H₂. Táto metóda je kľúčová pri výrobe priemyselných plynov vyžadujúcich vodík. Etanol sa tiež vyrába fermentáciou, ktorá môže uvoľňovať CO₂ a metán.
- Peroxid vodíka (H₂O₂): Peroxid vodíka je silné oxidačné činidlo. Jeho primárnym mechanizmom tvorby plynu je rozklad na vodu a kyslík: 2H₂O₂ → 2H₂O + O₂. Tento proces, najmä katalytický rozklad, produkuje vysoko čistý kyslík, ktorý je cenný v chemickom priemysle pre oxidačné reakcie a výrobu hnojív.
| Látka | Spôsob výroby plynu | Vzniknuté plyny | Typ reakcie |
|---|---|---|---|
| Izopropylalkohol | Spaľovanie | CO₂, H₂O | Exotermická reakcia |
| Pyrolýza | C₂H₄, CH₄, H₂O | Krakovacia reakcia pri vysokej teplote | |
| Etanol | Spaľovanie | CO₂, H₂O | Exotermická reakcia |
| Parné reformovanie | H₂, CO | Katalytická reakcia, parné reformovanie | |
| Fermentácia | CO₂ | Biochemická reakcia | |
| Peroxid vodíka | Rozklad | O₂ | Reakcia katalytického rozkladu |
Bezpečnostné Aspekty a Toxikológia
Páry izopropanolu sú ťažšie ako vzduch a sú ľahko zápalné v širokom rozsahu koncentrácií. Je nutné ho uchovávať mimo zdrojov tepla a otvoreného ohňa. Pri požití sa izopropanol rýchlo vstrebáva do tela. V pečeni sa metabolizuje na acetón, ktorý sa eliminuje oveľa pomalšie ako samotný izopropanol. Izopropanol silne dráždi oči a sliznice, spôsobuje útlm centrálneho nervového systému a vo vyšších dávkach aj útlm kardiovaskulárneho systému. Metabolit acetón tiež pôsobí tlmivo na CNS. Eliminácia acetónu môže vyvolať miernu acidózu. U potkanov bola zaznamenaná teratogenita. Karcinogénne ani mutagénne účinky neboli preukázané. Neexistuje špecifické antidotum; liečba je predovšetkým podporná a zameraná na udržanie životných funkcií a korekciu biochemických nerovnováh.
Je dôležité dodržiavať pokyny na skladovanie a manipuláciu s izopropanolom, najmä pri jeho použití ako paliva. Palivo by malo byť skladované na chladnom, suchom mieste mimo priameho slnečného žiarenia a potenciálnych zdrojov zapálenia, ideálne pri teplote 15-25 °C. Počas používania je potrebné palivo vložiť do vhodného horáka a nikdy sa nesnažiť doplniť horák, ktorý bol práve použitý, kým úplne nevychladne.
Všestrannosť izopropanolu, od čistiaceho prostriedku až po chemické palivo, podčiarkuje jeho význam v rôznych priemyselných a komerčných aplikáciách. Jeho spaľovanie je kľúčovým procesom, ktorý umožňuje využitie jeho energetického potenciálu a produkciu užitočných plynov.