Kuchynská soľ, bežný doplnok našich kuchýň a jedál, je viac než len dochucovadlo. Z chemického hľadiska je to soľ, konkrétnejšie chlorid sodný (NaCl). Soli ako trieda chemických zlúčenín sa vyznačujú kryštalickou štruktúrou tvorenou katiónmi kovov alebo amónnym iónom (NH₄⁺) a aniónmi kyslých radikálov. V prípade chloridu sodného sú to sodné ióny (Na⁺) a chloridové ióny (Cl⁻). Hoci drvivá väčšina solí tvorí kryštály, existujú aj výnimky, ako napríklad neštruktúrny difosfát cínatý (V) (Sn₂P₂O₇) alebo kvapalný fluorid antimónny (V) (SbF₅) pri izbovej teplote.
Názvoslovie solí vychádza z názvov kyselín, ku ktorým sa pridáva názov kovu a jeho mocenstvo. Názvy solí odvodených od hydrokyselín končia na "-id" (napr. chlorid), zatiaľ čo soli oxykyselín končia na "-át" (napr. síran). Pri tvorbe chemických názvov je dôležité uvádzať mocenstvo kyselinového radikálu a kovu. Pri dvojitých a trojitých soliach sa katióny uvádzajú v abecednom poradí s medzislovom "a", a predpona (di-, tri-) označuje počet atómov kovu. Prítomnosť vodíka v molekule soli je indikovaná predponou "hydro-", zatiaľ čo zásadité soli opisujú počet hydroxidových iónov. Hydratované soli, čiže hydráty, zahŕňajú celý názov soli a počet molekúl vody. Mnohé soli majú aj bežné, zaužívané názvy, ako napríklad sóda bikarbóna (kyselý uhličitan sodný) používaná pri pečení, kryštalická sadra (síran vápenatý (VI) - voda (1/2)) alebo čílsky ľadok (dusičnan sodný (V)).
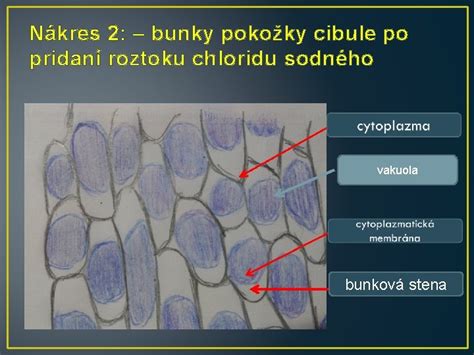
Soli tvoria iónové kryštály. Väčšina z nich je bezfarebná, pričom biela farba kryštálov často súvisí s ich fragmentáciou. Skutočná farba zlúčeniny závisí od mocenstva prvku. Hydratované soli sa môžu farebne líšiť od bezvodých foriem; napríklad chlorid kobaltnatý (CoCl₂) je modrý, ale jeho hydratovaná forma je ružová.
Rozpustnosť solí: Vplyv rozpúšťadla a teploty
Rozpustnosť solí vo vode je rôznorodá. Dusičnany, sodné, draselné a amónne soli sú vo všeobecnosti vo vode vysoko rozpustné a disociujú. Existuje však aj značná skupina solí, ktoré tvoria nerozpustné zrazeniny. Pri neistote sa odporúča použiť tabuľky rozpustnosti. Iónová disociácia solí vo vodných roztokoch je zodpovedná za ich elektrickú vodivosť - schopnosť prenášať elektrické náboje.
Rozpustnosť je kľúčová vlastnosť v mnohých priemyselných odvetviach a jej priebeh je výrazne ovplyvnený teplotou. Vo všeobecnom pravidle "podobné rozpúšťa podobné" platí, že polárne rozpúšťadlá rozpúšťajú polárne látky a nepolárne rozpúšťadlá rozpúšťajú nepolárne látky. Pre väčšinu pevných látok v kvapalných rozpúšťadlách platí, že s rastúcou teplotou sa rozpustnosť zvyšuje, pretože proces rozpúšťania je často endotermický (absorbuje teplo). Príkladom je kuchynská soľ (NaCl), ktorej rozpustnosť vo vode rastie s teplotou. Existujú však aj výnimky, kde rozpustnosť klesá so zvyšujúcou sa teplotou, čo naznačuje exotermický proces rozpúšťania (uvoľňuje teplo), ako napríklad pri síran vápenatý (CaSO₄).
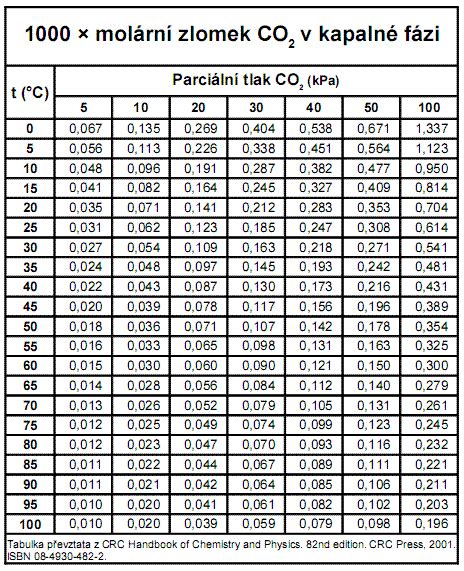
Pri rozpúšťaní kvapalín v kvapalinách môže teplota tiež ovplyvniť miešateľnosť. Rozpustnosť plynov v kvapalinách však vo všeobecnosti klesá so zvyšujúcou sa teplotou, pretože tento proces je exotermický. Typickým príkladom je sýtenie nápojov oxidom uhličitým.
Vplyv teploty na rozpustnosť je zásadný pre farmaceutický priemysel, kde určuje účinnosť liekov, ako aj pre chemickú výrobu pri procesoch separácie a čistenia. V potravinárstve a nápojovom priemysle sa využíva v procesoch ako varenie piva či výroba vína.
Kuchynská soľ a alkohol: Pohľad na rozpustnosť NaCl v etanolových roztokoch
Zatiaľ čo rozpustnosť kuchynskej soli (NaCl) vo vode je dobre zdokumentovaná, jej správanie v iných rozpúšťadlách, ako je etanol (etylalkohol), si zaslúži pozornosť. Etanol je bezfarebná horľavá kvapalina, ktorá sa vyrába predovšetkým alkoholovým kvasením. Je to polárne rozpúšťadlo, hoci menej polárne ako voda.
Vo všeobecnosti platí, že rozpustnosť iónových zlúčenín ako NaCl je v polárnych rozpúšťadlách vyššia. Voda je vysoko polárna molekula, zatiaľ čo etanol je menej polárny. Preto sa očakáva, že rozpustnosť NaCl vo čistom etanole bude výrazne nižšia ako vo vode. Voda je vynikajúce rozpúšťadlo pre NaCl vďaka svojej schopnosti solvatovať sodné ióny (Na⁺) a chloridové ióny (Cl⁻) prostredníctvom silných dipól-iónových interakcií. Etanol síce dokáže čiastočne solvatovať tieto ióny, ale jeho nižšia polarita a slabšie interakcie vedú k obmedzenej rozpustnosti.

Pri miešaní vody a etanolu vznikajú roztoky s rôznou polaritou v závislosti od zloženia. V zmesiach vody a etanolu sa rozpustnosť NaCl bude meniť. Pri nízkych koncentráciách etanolu vo vode bude rozpustnosť NaCl blízka rozpustnosti vo vode. S rastúcou koncentráciou etanolu sa však polarita roztoku znižuje, čo vedie k poklesu rozpustnosti NaCl. V čistom etanole je NaCl prakticky nerozpustný.

Vplyv teploty na rozpustnosť NaCl v etanole alebo v jeho zmesiach s vodou je tiež relevantný, hoci menej výrazný ako v prípade vody. Vo všeobecnosti platí, že pre väčšinu pevných látok, vrátane solí, sa rozpustnosť v organických rozpúšťadlách zvyšuje s rastúcou teplotou. Avšak kvôli nízkej základnej rozpustnosti NaCl v etanole, tento efekt nemusí byť taký markantný.
Je dôležité poznamenať, že "alkohol" ako bežný termín často odkazuje na etanol, ale môže sa použiť aj na iné alkoholové zlúčeniny. V kontexte kuchynskej soli a rozpustnosti je etanol najrelevantnejším alkoholom na zváženie.
Praktické dôsledky a aplikácie
Nízka rozpustnosť kuchynskej soli v etanole má praktické dôsledky. V procesoch, kde sa používa etanol ako rozpúšťadlo, napríklad pri extrakcii niektorých organických látok alebo pri výrobe liehovín, môže byť prítomnosť NaCl minimálna alebo môže viesť k jeho zrážaniu. Naopak, v procesoch, kde je žiaduca vysoká rozpustnosť solí, sa preferujú polárnejšie rozpúšťadlá ako voda.
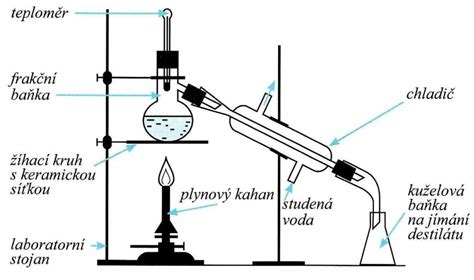
V chemickom priemysle sa pri oddeľovaní látok využíva rozdielna rozpustnosť. Napríklad pri purifikácii etanolu sa často používa destilácia. Vzhľadom na nízku rozpustnosť NaCl v etanole, by mohlo byť teoreticky možné oddeliť tieto látky pomocou destilačných techník, kde by sa etanol odparil ako prvá, zatiaľ čo soľ by zostala ako zvyšok.
Pochopenie rozpustnosti solí v rôznych rozpúšťadlách je kľúčové pre optimalizáciu chemických procesov, formuláciu produktov a predikciu správania sa látok v rôznych podmienkach. Hoci kuchynská soľ je vo vode výborne rozpustná, jej interakcia s alkoholom je výrazne obmedzená, čo odráža základné princípy chemickej rozpustnosti založené na polarite a intermolekulárnych silách.